STTT:信迪利单抗+西达本胺治疗复发/难治ENKTL的I/II期SCENT研究
2024-05-20 聊聊血液 聊聊血液 发表于上海
中山大学肿瘤防治中心黄慧强教授牵头一项1b/2期研究,评估了信迪利单抗联合西达本胺治疗38例RR-ENKTL患者的安全性和有效性,并探索性进行了生物标志物分析。
ENKTL
复发或难治性结外NK/T细胞淋巴瘤(RR-ENKTL)的预后较差,5年生存率不足30%。抗PD-1单抗在RR-ENKTL中可产生较高缓解率,但完全缓解率(CR)和反应持续时间(DOR)均有待提高,需要探索新的治疗方法与免疫疗法的结合。表观遗传药物与PD-1单抗具有协同作用,因此结合表观遗传学药物可能是一种潜在的治疗策略,以提高免疫治疗对RR-ENKTL的疗效。
中山大学肿瘤防治中心黄慧强教授牵头一项1b/2期研究,评估了信迪利单抗联合西达本胺治疗38例RR-ENKTL患者的安全性和有效性,并探索性进行了生物标志物分析。研究结果近日发表于《Signal Transduction and Targeted Therapy》。

研究方法&结果
研究方法
该研究为多中心、单臂、开放标签1b/2期研究,纳入18-75岁、组织学证实、天冬酰胺酶为基础方案或放化疗后复发或难治的ENKTL(WHO分类)。
治疗期包括两个阶段,1b期和2期扩展期。剂量递增阶段采用标准3+3设计,确定第一周期西达本胺的最大耐受剂量(MTD)、剂量限制性毒性(DLT)和确定推荐的II期剂量(RP2D)。在1b期,患者接受每周2次递增剂量的口服西达本胺(20、25和30mg),同时每21天静脉注射一次固定剂量的200mg信迪利单抗。
在2期部分,患者每21天接受固定剂量的200mg 信迪利单抗+西达本胺(RP2D)。CR或PR患者继续联合治疗,直到疾病进展、死亡、无法耐受的毒性或撤回同意,最长12个月(18个总周期);12个月后可选择维持治疗、停止治疗或移植。2期分为1个阶段,第1阶段入组7例患者,如果有4例患者缓解,则第2阶段继续入组21例患者,共28例。
预期联合治疗的客观缓解率(ORR)为80%。
患者特征
共入组38例患者(治疗人群)并接受至少1剂治疗(图1)。
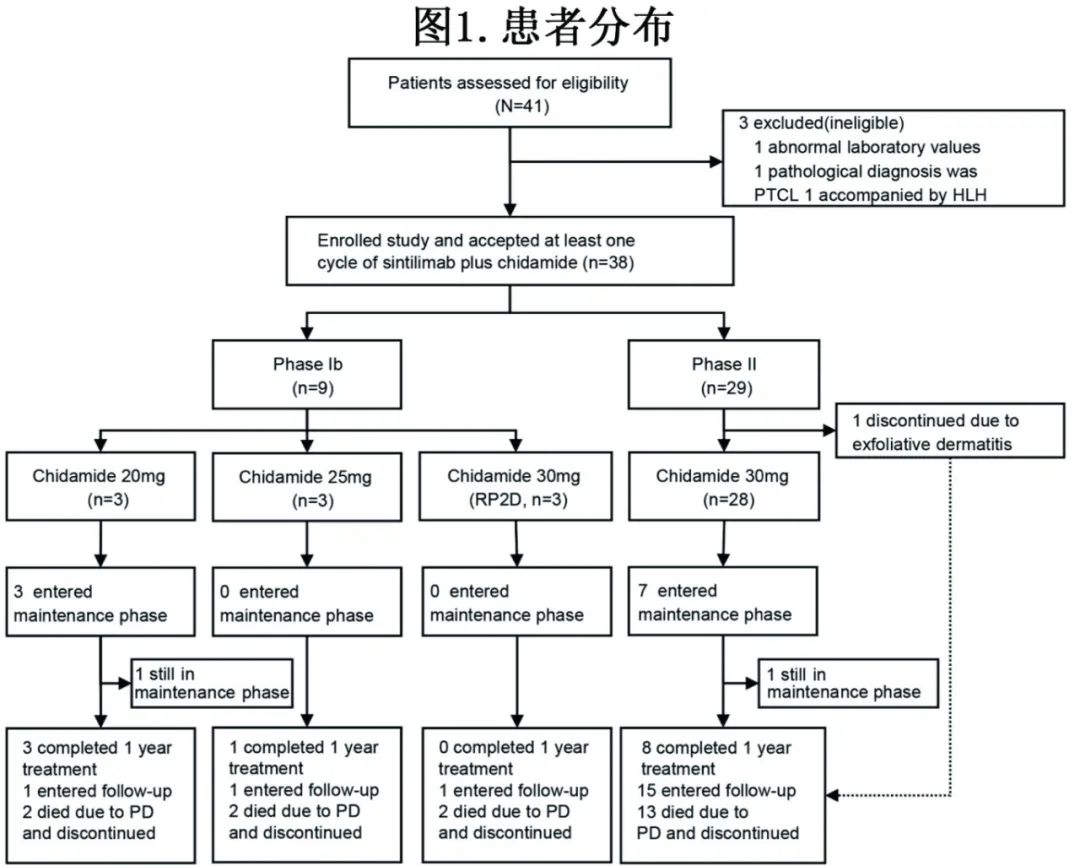
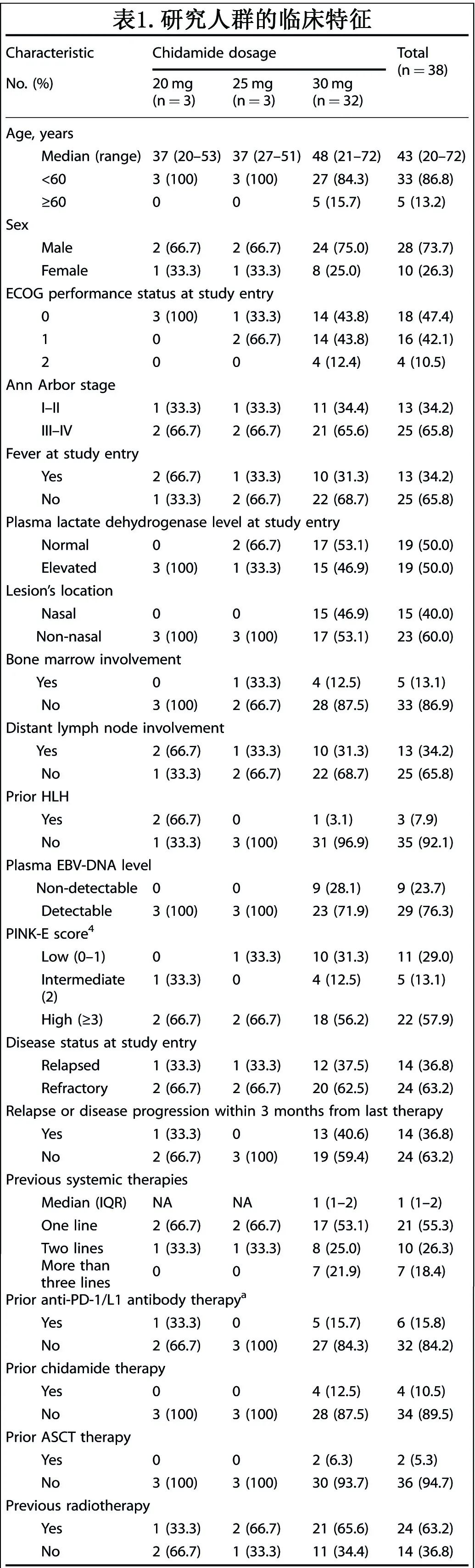
所有38例患者均纳入安全性分析,意向治疗人群(n=37)包括31例疗效可评估、接受推荐的2期剂量(RP2D)治疗的患者。基线特征见表1。总体而言,中位年龄为43岁,25例(65.8%)筛查时为III-IV期,22例(57.9%) PINK-E评分≥3,17例(44.7%)既往接受过≥2线全身治疗。从末次治疗到本研究的中位时间为6.5个月。14例(36.8%)患者从末次治疗到入组的中位间隔时间小于3个月。
疗效
1b期共9例患者,西达本胺20、25和30mg剂量组各3例,同时联合信迪利单抗固定剂量200 mg。未发生DLT,因此MTD为30mg,西达本胺的RP2D为30mg每周两次。2期部分有29例患者,接受西达本胺的RP2D联合信迪利单抗200mg。共32例患者接受西达本胺30mg治疗。
在1b期,9例患者中有6例缓解(ORR:66.7%),5例(55.6%)获得CR。在2期第一阶段入组8例患者,7例患者的疗效可评估;ORR为85.7%(6/7),5例患者(71.4%)达到CR,超过了预定的第二阶段入组疗效边界。在2期所有28例2期患者中,16例获得缓解,ORR为57.1% (16/28),CR率为46.4%(13/28)。在意向治疗人群(n=37)中,22例患者(59.5%)达到客观缓解,其中18例(48.6%)CR(表2)。10例患者接受过检查点抑制剂(ICI)(6例)或西达本胺(4例)治疗,信迪利单抗联合西达本胺治疗后,分别有6例(60.0%,6/10)和4例(40.0%,4/10)患者获得ORR和CR。
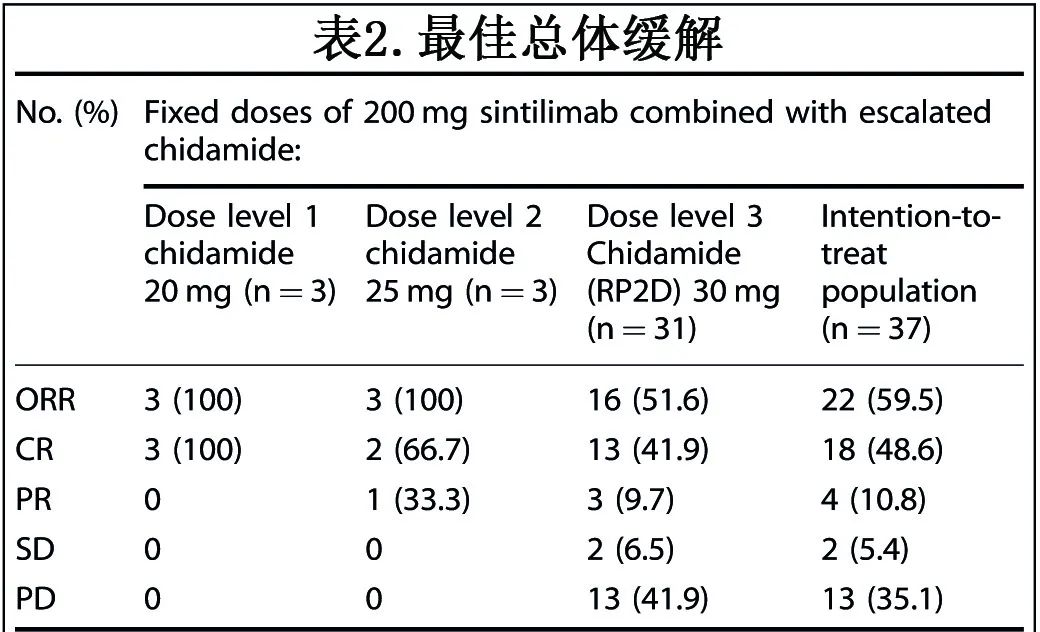
中位随访38.7个月。在22例缓解患者中,中位至缓解时间(TTR)为1.5个月,中位DOR为25.3个月。接受治疗人群的中位PFS为23.2个月,中位OS为32.9个月 (图2a, b),36个月 OS和PFS率分别为47.4% 和38.8%。获得CR或部分缓解(PR)的患者的生存率明显优于疾病稳定(SD)或进展性疾病(PD)的患者(图2c, d)。
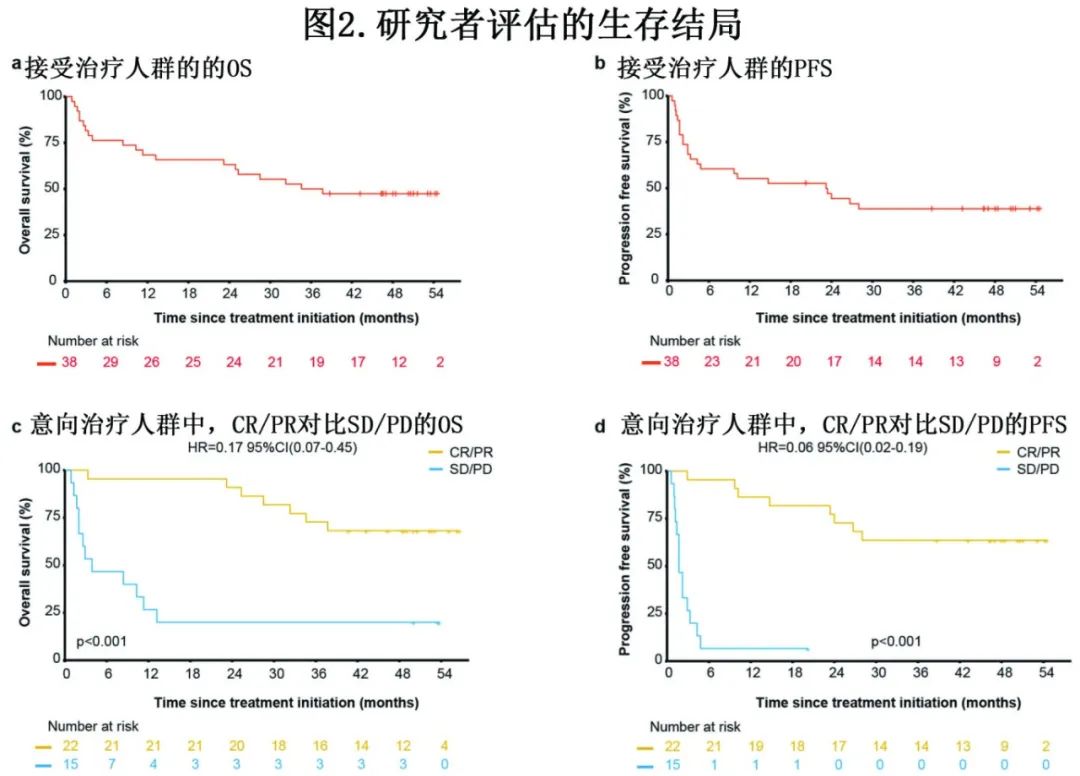
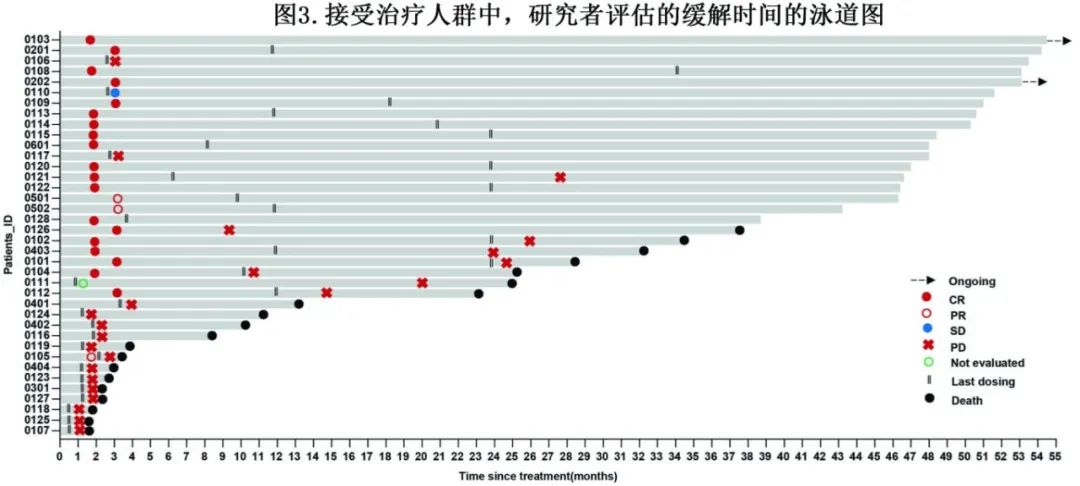
多因素分析显示,ECOG评分为2分(p=0.008)、骨髓受累(p=0.032)与较差的OS相关,ECOG评分为2 (p=0.018)、远处淋巴结受累(p=0.044)与PFS较差相关。2例(5.2%)患者接受信利迪单抗联合西达本胺作为维持治疗,没有患者接受自体造血干细胞移植(ASCT)(图3)。接受治疗的人群和缓解持续超过1年人群的中位周期分别为6和25。3例(7.8%)患者出现超进展(HPD),HPD的中位OS为1.3个月。
探索性生物标志物评估
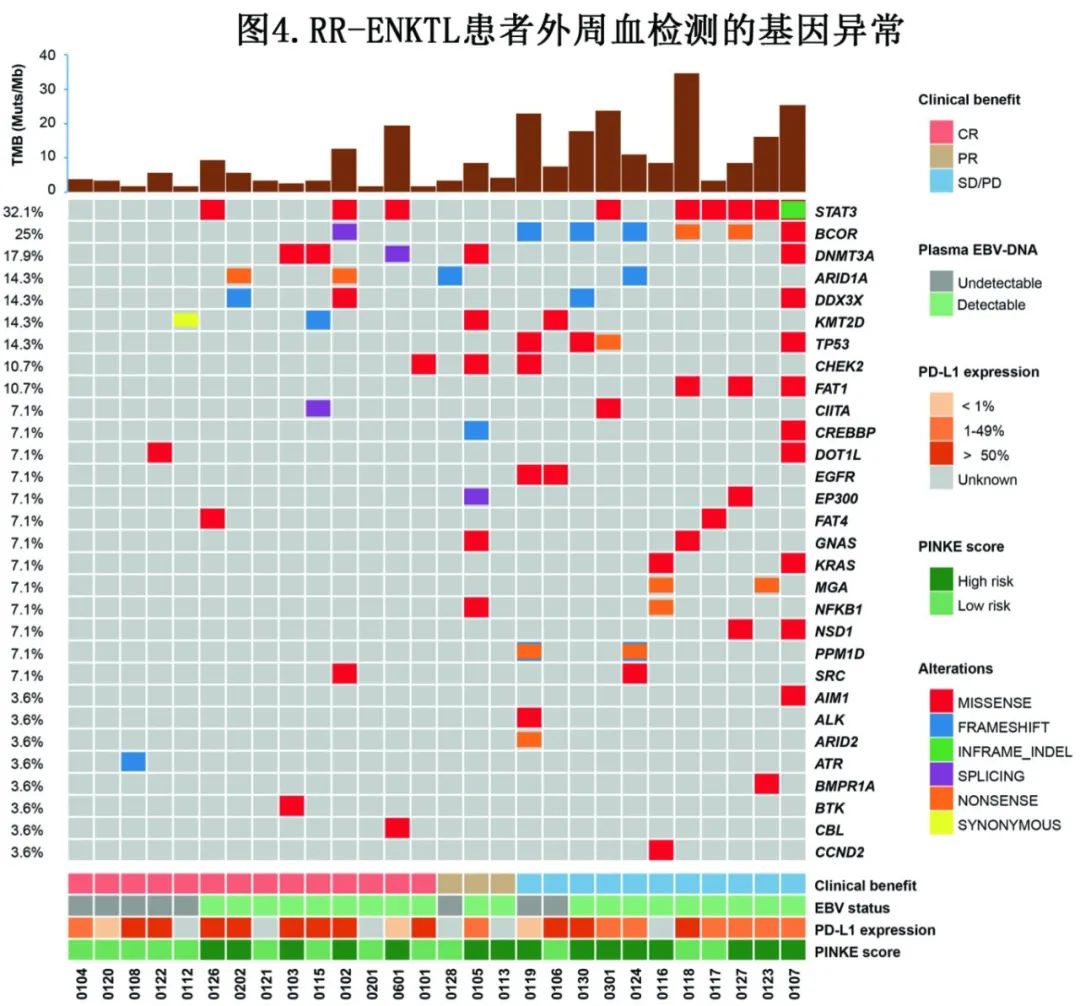
在28例可获得福尔马林固定石蜡包埋组织标本和外周血的患者中,有12例(42.8%)PD-L1表达超过50%,采用预测ORR的受试者工作特征(ROC)曲线确定截止值。综合阳性评分(CPS)中位值为50,截止值为32.5。中位肿瘤突变负荷(TMB)为5.6 mut/Mb,临界值为6.5 mut/Mb。治疗前外周血中常见(>10%)突变包括STAT3 (n=9)、BCOR (n=7)、DNMT3A (n=5)、ARID1A (n=4)、DDX3X (n=4)、KMT2D (n=4)、TP53 (n=4)、CHEK2 (n=3)和FAT1 (n=3),见图4。
单因素分析发现,PD-L1表达≥25%、CPS≥32.5、TMB <6.5Mb的患者ORR高于其他患者, TMB <6.5Mb与预后良好相关。对28例患者167份血浆样本进行动态循环肿瘤DNA (ctDNA)分析和定量,中位检测数为5。信迪利单抗联合西达本胺治疗未缓解的患者中ctDNA持续呈阳性。
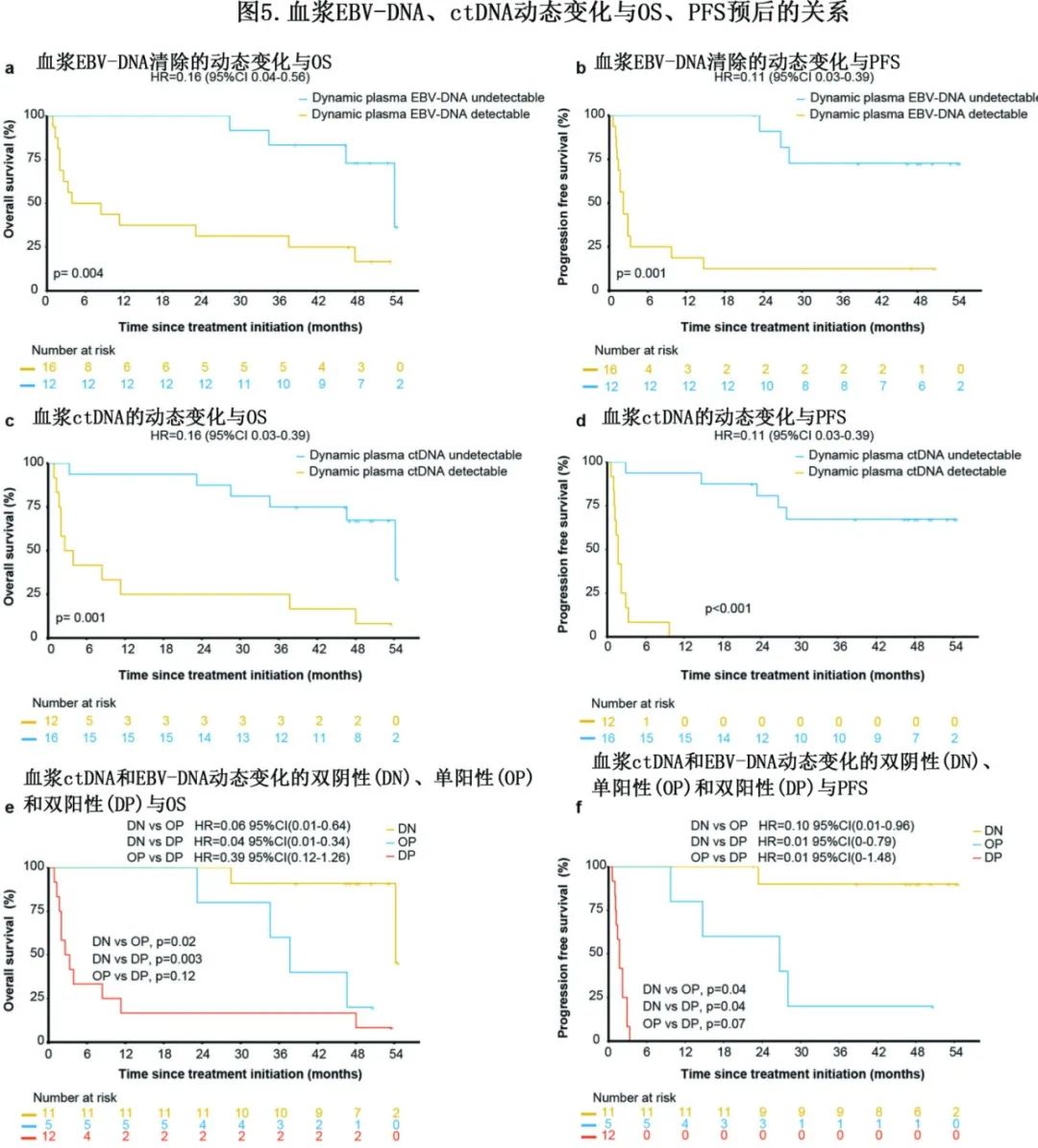
还评估了1年内动态血浆EB病毒(EBV)-DNA变化的作用,发现EBV-DNA在缓解患者中下降得更明显,直到检测不到,而未缓解的患者中EBV-DNA持续升高或保持不变。动态血浆ctDNA结合EBV-DNA比单独ctDNA或EBV-DNA可以更好地预测预后(图5a-f)。
单因素分析显示,与OS显著相关的基因有STAT3 (p=0.014)、BOCR (p=0.001)、FAT1 (p=0.001)、EP300 (p=0.02)、KRAS (p=0.02)、CREBBP (p=0.01)、NSD1 (p=0.002),与PFS显著相关的基因有STAT3 (p=0.006)、BCOR (p < 0.001)、PPM1D (p=0.02)、KRAS (p=0.02)、CREBBP (p=0.04)、NSD1 (p=0.003)、GNAS (p=0.05)。在多因素分析中,STAT3是OS和PFS的独立预后因素。
收集了27例患者的治疗前基线血清T细胞淋巴细胞亚群和Th1/Th2细胞因子,发现下列患者从信迪利单抗联合西达本胺治疗中获益更多:CD4+/CD8+比值较高(>0.71)、CD19+较高 (>7.8)、CD3+CD8+较低(≤34)、血浆IL-6水平较低(≤2.5 pg/mL)、IL-10水平较低(≤8.5 pg/mL)。
安全性
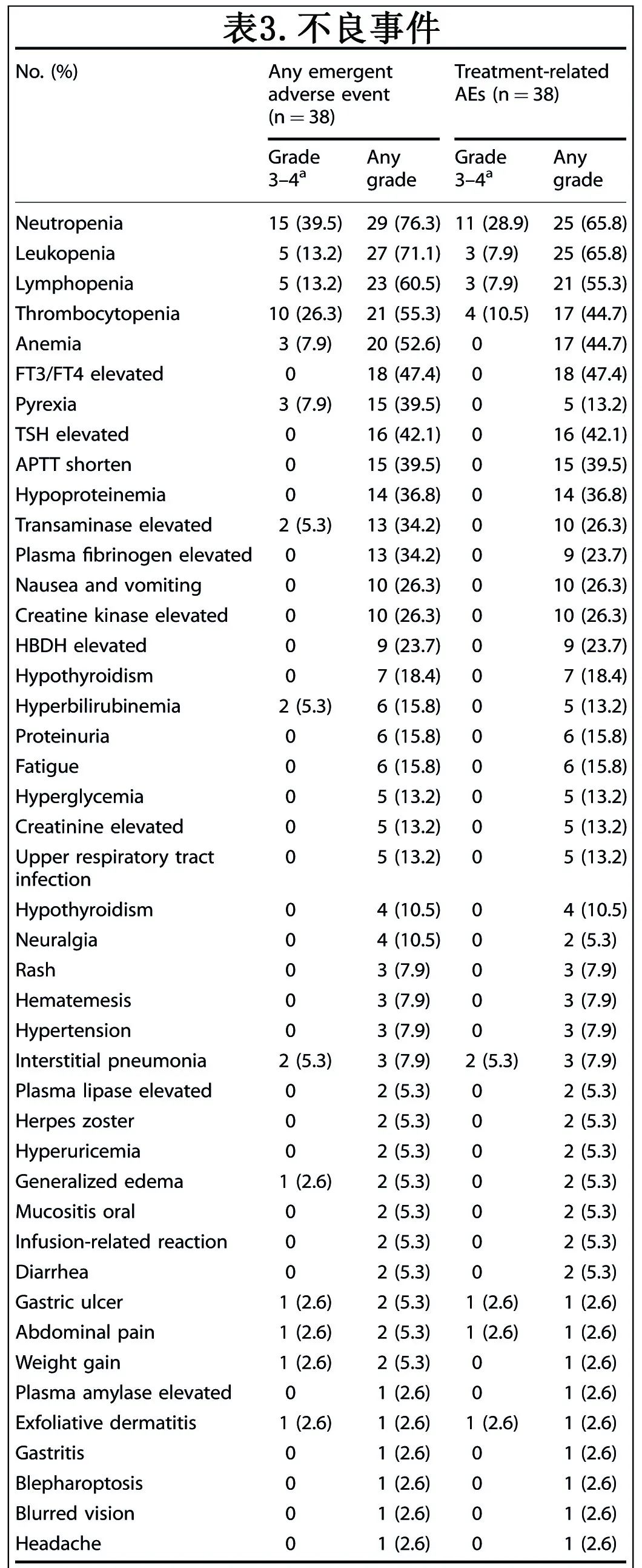
治疗相关不良事件(TRAE)见表3。38例(100%)患者报告TRAE。最常见的TRAE(≥20%)包括中性粒细胞减少症(65.8%)、血小板减少症(44.7%)、贫血(44.7%)、甲状腺功能减退症(47.4%)、APTT缩短(39.5%)、低蛋白血症(36.8%)、转氨酶水平升高(26.3%)、恶心和呕吐(26.2%)、肌酸激酶升高(26.3%)、血浆纤维蛋白原升高(23.7%)和羟基丁酸脱氢酶升高(23.7%)。最常见的≥3级TRAE(≥10%)为中性粒细胞减少症(28.9%)和血小板减少症(10.5%)。18例(47.4%)患者报告免疫相关不良事件(irAE),包括1例4级中毒性表皮坏死松解和1例间质性肺炎。最常见的irAE为1级甲状腺功能减退和皮疹。研究不推荐预防性药物治疗,也没有进行预防性药物治疗。联合治疗中未发现既往治疗的毒性明显增加。2例(5.3%)患者发生导致永久性停药的TRAE。没有死亡与研究药物有关。
总结
该1b/2期研究中,预期联合治疗的客观缓解率(ORR)为80%。患者接受递增剂量的西达本胺,与固定剂量信迪利单抗联合用药,周期21天,最长可达12个月。未观察到剂量限制性毒性,西达本胺的RP2D为30mg每周2次。2期研究部分共纳入29例患者。在意向治疗人群(n=37)中,ORR为59.5%,CR率为48.6%。中位DOR、PFS和OS分别为25.3个月、23.2个月和32.9个月。最常见的≥3级TRAE为中性粒细胞减少症(28.9%)和血小板减少症(10.5%),18例(47.3%)患者报告与免疫相关AE。探索性生物标志物评估表明,动态血浆ctDNA结合EBV-DNA在预后中起着重要作用。此外STAT3突变预后不良。
虽然没有达到预期的ORR,但信迪利单抗联合西达本胺具有可控的安全性,并且首次在RR-ENKTL中产生较高的CR率和DOR。对于这一人群来说,信迪利单抗联合西达本胺是一种很有前途的治疗选择,表观遗传调节剂与抗pd -1单抗协同作用可显著增强RR-ENKTL治疗的抗肿瘤效果。此外动态血浆ctDNA联合EBV-DNA可发挥重要的预后作用。
参考文献
Gao, Y., He, H., Li, X. et al. Sintilimab (anti-PD-1 antibody) plus chidamide (histone deacetylase inhibitor) in relapsed or refractory extranodal natural killer T-cell lymphoma (SCENT): a phase Ib/II study. Sig Transduct Target Ther 9, 121 (2024). https://doi.org/10.1038/s41392-024-01825-0
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#西达本胺# #结外NK/T细胞淋巴瘤# #信迪利单抗# #ENKTL#
8