Circulation:PAH患者中血浆细胞游离DNA预测其存活率并映射其损伤来源
2022-11-13 肺动脉高压研究进展 肺动脉高压研究进展
肺动脉高压(PAH)的风险预测仍然是一个重大挑战。缺乏疾病特有的替代生物标志物,导致继续依赖主观功能评估和有创血流动力学测量。
 肺动脉高压(PAH)的风险预测仍然是一个重大挑战。缺乏疾病特有的替代生物标志物,导致继续依赖主观功能评估和有创血流动力学测量。因此,PAH疾病进展的新型无创生物标志物仍然是一个未得到满足的需求,特别是如果这种生物标志物与PAH发病机制的程度有合理的关系,并能提供重要的信息。
肺动脉高压(PAH)的风险预测仍然是一个重大挑战。缺乏疾病特有的替代生物标志物,导致继续依赖主观功能评估和有创血流动力学测量。因此,PAH疾病进展的新型无创生物标志物仍然是一个未得到满足的需求,特别是如果这种生物标志物与PAH发病机制的程度有合理的关系,并能提供重要的信息。
已经对PAH的几个血清生物标志物进行了研究。然而,临床上广泛接受的程度有限,也许是因为它们缺乏特异性,与PAH发病机制的联系不明确。事实上,目前只有BNP(脑钠肽)及其前体NT-proBNP(N-末端probrain-type natriuretic pep-tide)被用于PAH风险评分中。虽然BNP和NT-proBNP与右心室失代偿和容量负荷有关,但它们并不代表目前的PAH病理病变程度,包括遗传和表观遗传因素、内皮损伤和破坏、代谢紊乱与高增殖、抗凋亡的细胞表型,以及全身和局部失调的炎症。
无细胞DNA(cfDNA)是循环的短DNA片段(≈165个碱基对),主要来自单核糖体,代表细胞损伤或细胞周转。此外,cfDNA作为实体器官移植排斥反应的无创标志物以及肿瘤学中的基因分型和监测工具,已具有临床意义。高通量甲基化测序技术的进步也使cfDNA亚群在起源细胞的基础上得到区分,有利于检测细胞或组织的特定损伤。
鉴于PAH的发病机制与以细胞增殖增加为特征的疾病(如癌症)和以炎症为媒介的组织损伤(如异体移植排斥)相似,本研究试图确定PAH患者的血浆cfDNA浓度是否升高,是否与PAH疾病严重程度相关,并预测结果。
研究方法:
在2个PAH队列(A,n=48;B,n=161)和对照组(n=48)测量血浆cfDNA。收集的数据用于REVEAL 2.0(评估早期和长期PAH疾病管理的注册表)的评分和结果测定。患者被分为以下REVEAL风险组:低(≤6)、中(7-8)和高(≥9)。通过单因素方差分析比较对照组和PAH风险组之间的cfDNA总浓度。Log-rank测试比较了cfDNA分层和REVEAL风险组之间的生存率。队列B(n=96)和对照组(n=16)的样本子集进行了亚硫酸氢盐测序,然后采用去卷积算法绘制细胞特异性cfDNA甲基化模式,用t检验比较浓度。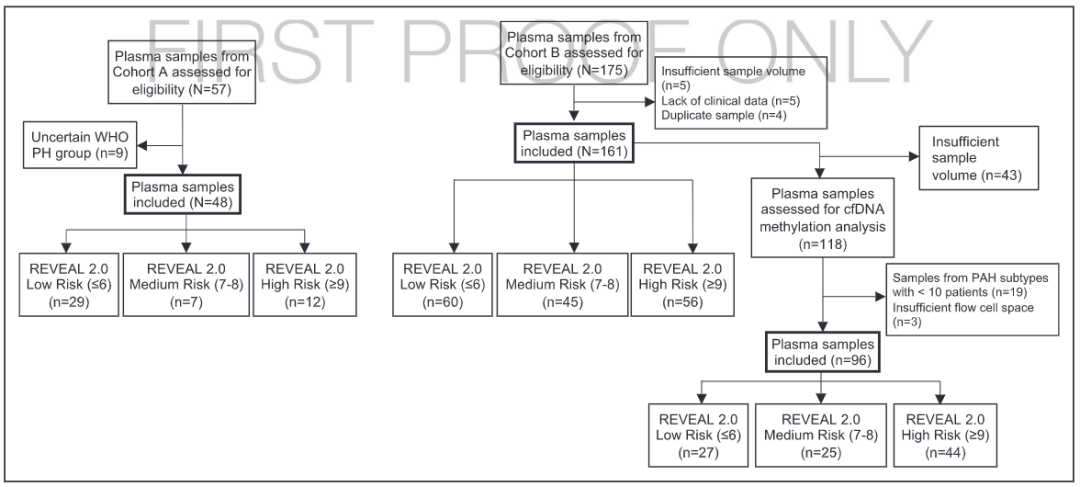 图1.患者流程图。选择用于无细胞DNA(cfDNA)甲基化分析的血浆样本(n=96)来自特发性肺动脉高压(IPAH;n=42)、与结缔组织疾病(CTD;n=35)相关的肺动脉高压(PAH)或与门静脉高压(PoHTN;n=19)相关的肺动脉高压患者。
图1.患者流程图。选择用于无细胞DNA(cfDNA)甲基化分析的血浆样本(n=96)来自特发性肺动脉高压(IPAH;n=42)、与结缔组织疾病(CTD;n=35)相关的肺动脉高压(PAH)或与门静脉高压(PoHTN;n=19)相关的肺动脉高压患者。
研究结果:
在队列A中,中位数(四分位数范围)年龄为62岁(47-71),75%为女性,而REVEAL 2.0中为6(4-9)。在队列B中,中位数(四分位数范围)年龄为59岁(49-71),69%为女性,而REVEAL 2.0中为7(6-9)。在这两个队列中,不同REVEAL风险的PAH患者和对照组的cfDNA浓度不同(方差分析P≤0.002),与低风险类别相比,高风险患者的cfDNA浓度更高(P≤0.002)。
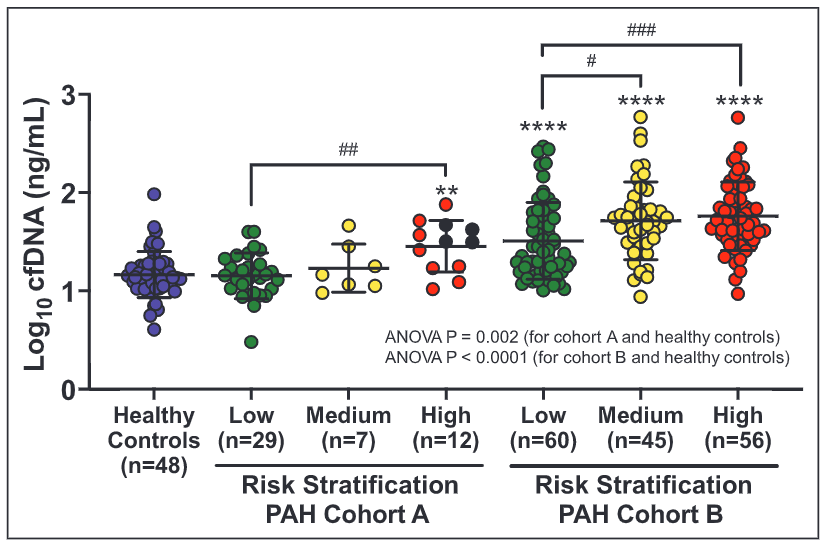 图2.PAH患者的cfDNA浓度升高,并与两个独立的患者队列中的REVEAL 2.0风险评分相关。
图2.PAH患者的cfDNA浓度升高,并与两个独立的患者队列中的REVEAL 2.0风险评分相关。
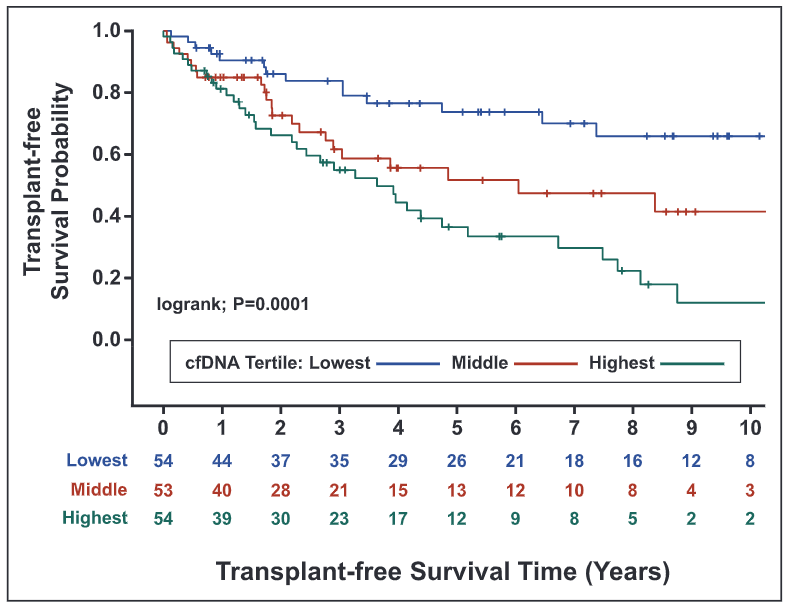 图3.队列B中cfDNA浓度升高与较低的无移植生存率有关。
图3.队列B中cfDNA浓度升高与较低的无移植生存率有关。
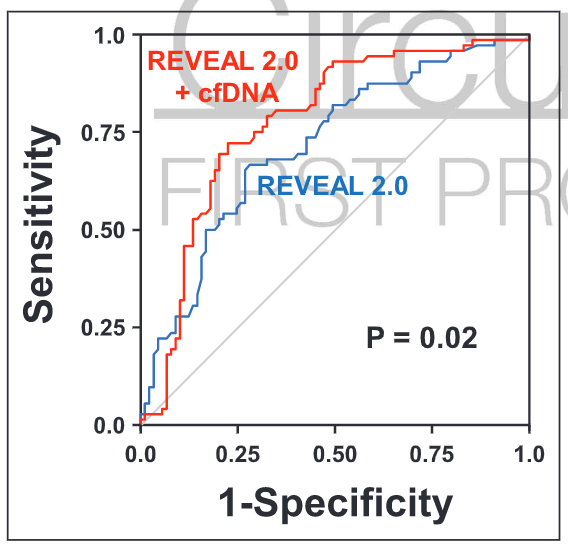 图4.REVEAL 2.0风险和REVEAL 2.0风险的接受者操作特征分析,加上cfDNA预测B组的死亡或肺部移植。
图4.REVEAL 2.0风险和REVEAL 2.0风险的接受者操作特征分析,加上cfDNA预测B组的死亡或肺部移植。
在队列B中,最低、中间和最高cfDNA分层的54名患者中有14名死亡或肺移植,53名中有23名,54名中有35名。cfDNA水平分层为分层(log-rank:P=0.0001)和REVEAL风险组(log-rank:P<0.0001)分别预测无移植生存。在REVEAL中加入cfDNA可改善辨别能力(接收者操作特征曲线下的面积,0.72-0.78;P=0.02)。
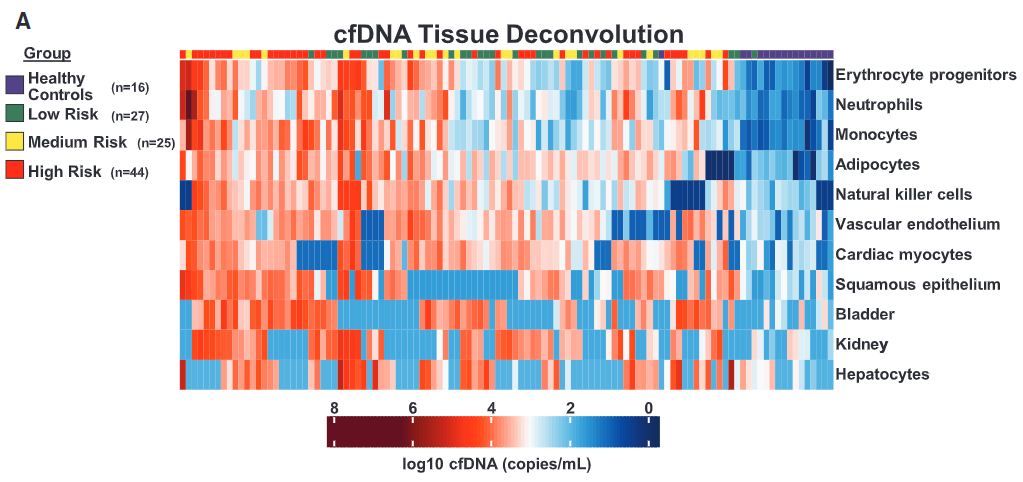
图5.PAH患者表现出明显的、有病理意义的cfDNA损伤模式。
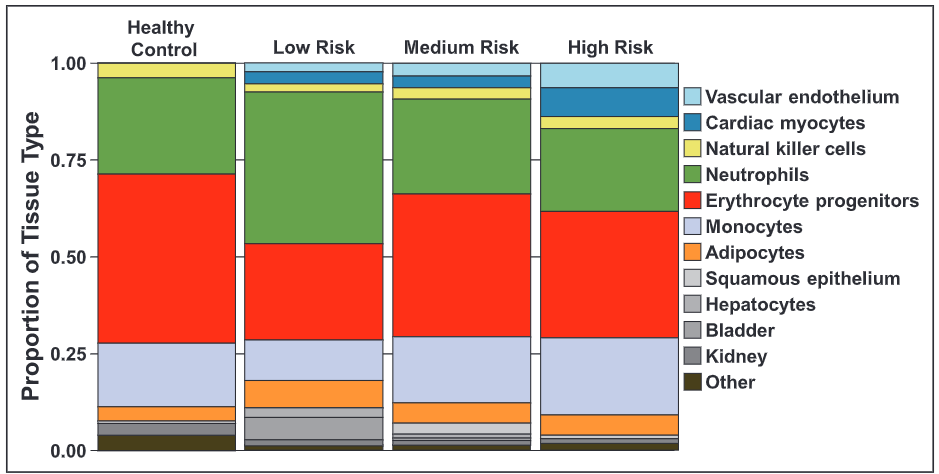 图6.来自健康对照组和低、中、高风险的PAH患者的代表性cfDNA分布情况。
图6.来自健康对照组和低、中、高风险的PAH患者的代表性cfDNA分布情况。
与对照组相比,PAH患者的甲基化分析显示,源自红细胞祖细胞、中性粒细胞、单核细胞、脂肪细胞、自然杀伤细胞、血管内皮和心肌细胞的cfDNA增加。来自红细胞祖细胞、心肌细胞和血管内皮的cfDNA浓度在高风险与低风险REVEAL评分的PAH患者中更大(P≤0.02)。
研究总结及临床前景:
- 与健康对照组相比,肺动脉高压患者的循环无细胞DNA(cfDNA)升高了。
- 在2个独立的肺动脉高压患者队列中,cfDNA的浓度随着疾病的严重程度而增加,并预测2个队列中较大的队列的无移植生存率。
- 甲基化模式显示,增加的cfDNA来自生物学上合理的部位,包括红血球祖细胞和骨髓系炎症细胞、血管内皮和心肌细胞。
- cfDNA浓度可作为肺动脉高压患者潜在疾病活动的非侵入性生物标志物。
- cfDNA测量可为目前使用的肺动脉高压风险评分增加预后价值。
- 按组织来源分类的cfDNA可能为了解肺动脉高压的发病机制提供一个独特的、无创的窗口。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







