Cell Res:浙江大学王建安等团队合作发现靶向促炎T细胞作为潜在解决人类动脉粥样硬化的新治疗方法
2024-03-19 iNature iNature 发表于上海
该研究表明针对T细胞的免疫治疗可能是解决人类AS的有效策略。
动脉粥样硬化(AS)是全球心脑血管疾病的主要原因,其发展受到脂质含量积聚和慢性炎症的驱动。传统策略主要侧重于降低脂质以控制AS的进展,而留下残留的炎症风险导致主要不良心血管事件(MACEs)。尽管针对先天免疫的抗炎疗法已经减少了MACEs,但许多患者仍然面临重大风险。AS进展的另一个关键因素是适应性免疫,但其在预防AS方面的潜在作用尚不清楚。
2024年3月15日,浙江大学王建安、陈伟、尹巍巍及胡新央共同通讯在Cell Research在线发表题为“Targeting pro-inflammatory T cells as a novel therapeutic approach to potentially resolve atherosclerosis in humans”的研究论文,该研究对患有AS斑块的肿瘤患者进行了回顾性队列研究。该研究发现,抗程序性细胞死亡蛋白1(PD-1)单克隆抗体(mAb)显著减少AS斑块的大小。通过多组学单细胞分析,该研究全面表征了AS斑块特异性PD-1+ T细胞,这些细胞被激活并具有促炎作用。
该研究证明,当抗PD-1 mAb被髓样细胞表达的Fcγ受体(FcγRs)捕获时,它与T细胞上表达的PD-1相互作用。这种相互作用将抗PD-1 mAb转化为替代PD-1配体,在AS斑块的PD-1配体缺失环境中抑制T细胞功能。此外,该研究对接受抗PD-1 mAb治疗的肿瘤患者进行了前瞻性队列研究,其中一些患者具有Fc结合能力,而另一些没有。该研究显示,具有Fc结合能力的抗PD-1 mAb有效减少AS斑块的大小,而没有Fc结合能力的抗PD-1 mAb则没有。总之,该研究表明针对T细胞的免疫治疗可能是解决人类AS的有效策略。

动脉粥样硬化(AS)是一种慢性疾病,导致临床并发症,即主要不良心血管事件(MACEs),是全球主要死亡原因。它的特征是在较大动脉的内膜空间中过度脂质沉积,低密度脂蛋白胆固醇(LDL-C)的滞留引发动脉炎症。到目前为止,最常见的临床治疗方法是使用降脂药物(如他汀类药物)有效降低血脂水平。强化降脂药物可以有效减少MACE的发生率30%,但许多患者仍然会发生MACE。接近40%的患者患有MACE已经将其总胆固醇(TC)水平降至正常水平,这表明仅降低脂质远远不足以消除AS患者MACE的发生。最近的一项多国试验研究分析了接受他汀治疗的患者,并报告MACE的发生主要与残留的炎症风险(高C-反应蛋白(CRP))相关,而不是残留的胆固醇风险(高LDL-C),这表明仅使用他汀类药物不足以预防MACE。
慢性和低级别炎症在动脉粥样硬化的所有阶段存在,既有先天免疫又有适应性免疫参与AS炎症的调节。招募和分化炎症巨噬细胞和负载脂质的泡沫细胞是AS斑块形成和成熟的重要因素。针对先天免疫,进一步干预人类动脉粥样硬化可能需要抗炎和降脂策略的合作以提高临床疗效。事实上,最近的临床试验已经显示通过针对先天免疫可以在减少MACE方面具有一定的疗效。例如,Canakinumab抗炎血栓形成结果研究(CANTOS)利用了一种组合使用降脂和抗炎药物的方法,如抗白介素(IL)-1β单克隆抗体(mAb),它中和了NLRP3 / IL-1β途径和促炎细胞因子的合成。随后的临床试验,如科科林心血管结局试验(COLCOT)和低剂量秋水仙素2试验(LoDoCo2),都表明低剂量秋水仙素(抑制微管聚合防止IL-1β产生)与他汀类药物同时使用可以进一步减少MACE的发生率约15%至30%。然而,解决残留的炎症风险仍有很大的改进空间,需要探索和识别更有效的免疫靶点。
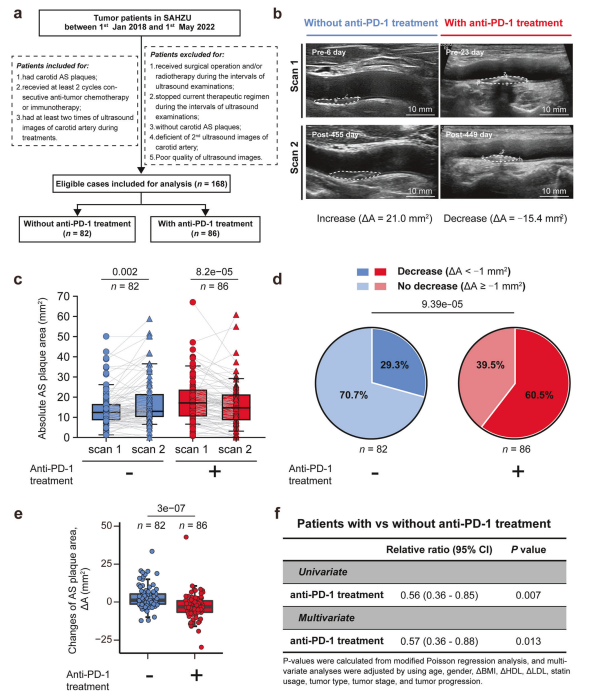
回顾性队列分析显示,抗PD-1治疗在体内阻碍并逆转AS斑块的进展(图片源自Cell Research )
适应性免疫是免疫系统的另一个重要分支,调节动脉粥样硬化中的炎症。然而,利用适应性免疫调节人类动脉粥样硬化仍然具有挑战性。越来越多的证据支持适应性免疫作为人类动脉粥样硬化的重要调节因子的因果作用。通过单细胞技术,先前的研究确定了T细胞作为浸润人类AS斑块的重要免疫细胞类型。针对人类AS斑块中呈现的局部抗原,T细胞通过与各种抗原提呈细胞(如泡沫细胞,巨噬细胞和树突状细胞)的相互作用,促进动脉粥样硬化的形成。
这些相互作用激活特异性抗原T细胞并克隆性扩展其T细胞受体(TCR)库,导致分化成多种亚群,并产生促炎细胞因子,促进AS的进展。另一方面,最近的单细胞分析报告称自反应CD4+ T细胞是驱动人类动脉粥样硬化的自身免疫成分。此外,AS斑块驻留的T细胞具有PD-1+亚群表现出“早期衰竭”表型,这可能表明这些T细胞不同于肿瘤中的完全衰竭,可能可调节以重塑T细胞应答。因此,作者建议这些T细胞可能是抑制人类AS斑块中T细胞介导的炎症反应的有价值靶点,但需要进一步研究。
该研究在接受抗PD-1治疗的肿瘤患者的回顾性队列中调查了抗PD-1治疗对AS斑块的临床效果。令人惊讶的是,作者发现抗PD-1治疗在减少人类AS斑块面积方面发挥了显著作用。此外,作者发现AS斑块特异性PD-1+ T细胞被激活并具有促炎作用。针对这些细胞可以在体外抑制T细胞反应。然后,作者解剖了其工作机制之一,即Fc结合抗PD-1 mAb可以被髓样细胞上的Fcγ受体捕获并作为“代理PD-1配体”抑制这些PD-1+ T细胞的激活。为了支持这种机制,该研究进一步对前瞻性队列进行了检查,发现只有具有Fc结合能力的抗PD-1 mAb才能有效减少AS斑块的大小,而没有Fc结合能力的抗PD-1 mAb则不能。
原文链接:
https://doi.org/10.1038/s41422-024-00945-0
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#靶向促炎T细胞# #动脉粥样硬化#
22