Nat Commun:徐州医科大学曹江等团队合作开发治疗复发/难治性多发性骨髓瘤的潜在新方法
2024-04-24 iNature iNature 发表于陕西省
该研究设计了靶向 BCMA/CD19的双特异性BC19 CAR T细胞,并评估了体外和体内的抗骨髓瘤活性。
尽管B细胞成熟抗原(BCMA)特异性嵌合抗原受体(CAR)T细胞疗法在复发难治性多发性骨髓瘤(R/R MM)中取得了很高的治疗效果,但单靶点免疫疗法存在原发性耐药和复发。
2024年4月20日,徐州医科大学曹江、徐开林及郑骏年共同通讯在Nature Communications发表题为“Bispecific CAR T cell therapy targeting BCMA and CD19 in relapsed/refractory multiple myeloma: a phase I/II trial”的研究论文,该研究设计了靶向 BCMA/CD19的双特异性BC19 CAR T细胞,并评估了体外和体内的抗骨髓瘤活性。临床前结果表明,BC19 CAR特异性识别靶抗原,BC19 CAR T细胞介导BCMA或CD19阳性癌细胞的选择性杀伤。BC19 CAR T细胞在异种移植小鼠模型中也表现出有效的抗原特异性抗肿瘤活性。研究在50名R/R MM患者中对BC19 CAR T细胞进行了一项开放标签、单臂、I/II期研究(ChiCTR2000033567)。主要终点是安全性。
BC19 CAR T 细胞耐受性良好,8%的患者出现3级或更高级别的细胞因子释放综合征,4%的患者出现1级神经毒性事件,达到预先指定的主要终点。次要终点包括总缓解率(92%)、中位无进展生存期(19.7个月)、中位总生存期(19.7个月)和中位缓解持续时间(未达到)。研究表明,双特异性 BC19 CAR T细胞在治疗R/R MM患者方面是可行、安全和有效的。

多发性骨髓瘤(MM)是第二常见的血液系统恶性肿瘤,其特征是骨髓中浆细胞的克隆性增殖或髓外产生单克隆免疫球蛋白的部位较少见。尽管过去十年的治疗取得了重大进展,提高了患者的生存率,但MM仍然被认为是无法治愈的,几乎所有MM患者最终都会复发。复发和难治性(R/R)MM患者的有效和可耐受的治疗方案仍然不令人满意,三难治性患者的中位总生存期(OS)为9.3个月,五难治性患者为5.6个月。
靶向B细胞成熟抗原(BCMA)的嵌合抗原受体(CAR)T细胞疗法在经过大量预处理和难治性MM患者中显示出有希望的反应和结果,总缓解率为48-100%,完全缓解率为6-76%。然而,一些患者对BCMA靶向CAR T细胞没有反应,或者在获得反应后不久复发。在CAR-T治疗后,4-33%的进行性患者观察到BCMA表达下调或缺失。解决这个问题的一种方法是使用双靶向CAR T细胞,正如在使用靶向CD19/CD22的CAR T细胞治疗白血病和淋巴瘤,靶向CD19/CD20的CAR T细胞治疗淋巴瘤,靶向BCMA/CD38的CAR T细胞治疗MM的临床试验中观察到的那样。
先前的研究表明,一小部分MM细胞表达CD19,CD19被认为是分化程度较低的MM细胞或骨髓瘤样干细胞,与耐药性和生存率低有关。最近的研究证实,在大多数患者中,CD19在一小部分骨髓瘤细胞(10.3-80%)上以超低密度表达,而CD19低骨髓瘤细胞可被抗CD19 CAR T细胞消除。此外,在大剂量美法仑和挽救性自体造血干细胞移植(Auto-HSCT)后给予抗 CD19 CAR T 细胞也显示出对 R/R MM 的潜在活性。人源化抗CD19和抗BCMA CAR T细胞的联合输注在复发/复发MM患者中是可行的。
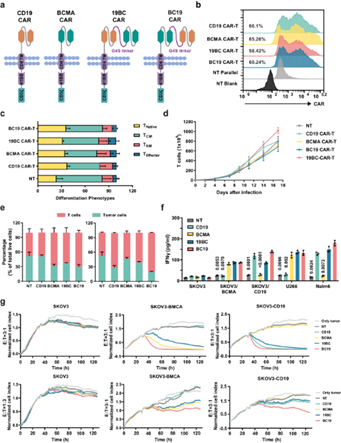
靶向BCMA或/和CD19的单特异性或双特异性CAR T细胞在体外的构建和功能验证(图源自Nature Communications )
基于这些初步数据,该研究设计了含有抗BCMA单链可变片段(scFv)和人源化抗CD19 scFv的第二代双特异性BC19 CAR。研究报告了双特异性BC19 CAR T细胞的临床前结果以及在I/II期试验中接受治疗的R/R MM患者的结局。50名R/R MM患者接受BC19 CAR T细胞输注。观察到BC19 CAR T细胞耐受性良好,表现出显着的临床疗效。该人群的总缓解率为92%,中位无进展生存期为19.7个月,1年总生存率为85%。总体而言,研究发现,输注BC19双特异性CAR T细胞是治疗R/R MM患者的一种可行、安全和有效的策略。
参考消息:
https://doi.org/10.1038/s41467-024-47801-8
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#多发性骨髓瘤# #CD19# #BCMA#
6