美国将CAR-T疗法纳入医保
近日,美国医疗保险和医疗补助服务中心(CMS)宣布同意为CAR-T疗法买单,即向医院支付数十万美元,用于CAR-T疗法治疗特定的癌症患者。
医谷 - CAR-T,医疗保险,癌症 - 2018-04-10
美国高价药的背后:美国药企暴涨药价,药企药品定价毫无约束
美国是世界上药价最贵的国家。据凯泽家庭基金会2016年的一项数据统计,有至少1900万美国成年人因国内药价过高而选择去加拿大或墨西哥等其他国家去买药。有美国媒体报道,某品牌胰岛素在美国标价274.7美
央视新闻 - 美国,高价药,约束 - 2020-09-11
美国新药特殊审评制度优秀经验借鉴
2018年,美国FDA共批准了59款新药,是近26年来新药核准数量最多的一年,从一个侧面反映出美国政府优化法规监管、加速新药上市的政策倾向。
火石创造 - 新药,特殊审批,法规监管,新药上市 - 2019-06-13
美国干细胞诊所发展现状
最近的一些资料显示,美国干细胞企业的网站数量迅速增长。有数百家干细胞公司正在做一系列干细胞疗法的直销广告。
阎影科学网博客 - 干细胞诊所,干细胞疗法,FDA - 2018-02-12
FDA对眼用制剂的质量研究要求及启示
该指导原则草案讨论了用于眼内和眼周局部给药的眼用产品,包括凝胶、软膏、乳膏和液体制剂等剂型的眼用制剂的一些质量考虑,涵盖质量研究中微生物学、可见颗粒物、可提取物和可浸出物、杂质和降解产物、稳定性研究等
药物评价研究 - FDA - 2024-05-20
FDA批准首个夜间尿频治疗药物Noctiva
3月3日,FDA宣布批准Noctiva(醋酸去氨加压素)鼻腔喷雾用于治疗夜间多尿导致至少起夜2次的成人尿频患者。这是FDA批准的第一个治疗夜间尿频的药物。FDA药品评价与研究中心(CDER)骨骼、生殖和泌尿产品办公室主任Hylton V.
医药魔方数据 - 夜间尿频,药物,治疗 - 2017-03-05
BMJ:美国非专利药物供应情况调查
研究发现,在美国超过一半的非专利药物缺少一般性竞争,是导致非专利药物短缺和价格上涨的重要因素
MedSci原创 - 药物,药价,非专利药物 - 2018-03-23
美国优先审查Sanofi,Regeneron的cemiplimab。
美国监管机构正在对Sanofi和的cemiplimab进行优先审查,以治疗转移性皮肤鳞状细胞癌(CSCC)的患者,或者是那些不能手术的局部晚期CSCC患者。晚期CSCC是最致命的非黑色素瘤皮肤癌,每年在美国造成约7000人死亡。目前没有FDA批准的治疗方法。Cemiplimab是一种针对检查点抑制剂PD-1的试验性人类单克隆抗体,去年在美国被授予突破性治疗的称号。该药物的市场提交数据包含来自关键的
MedSci原创 - cemiplimab,优先审查 - 2018-04-30
2021年9月19日简报:福建4地新增31例确诊病例;国药灭活疫苗在儿童中效果良好;美国FDA否决辉瑞新冠疫苗加强针计划
截至北京时间2021年9月19日7时01分,Worldometers世界实时统计数据显示,全球累计确诊新冠肺炎(COVID-19)病例超过22875万例,新增371,977例,达到228,754,79
MedSci整理 - 新冠疫苗 - 2021-09-19
柳叶刀社论:美国的种族主义,如何确保亚裔美国人的健康平等
在美国,实现卫生健康公平要求承认、理解并回应移民对社会的贡献,以满足不同群体和个人的不同需求,并消除对亚裔美国人的种族主义和歧视。
MedSci原创 - 2021-04-04
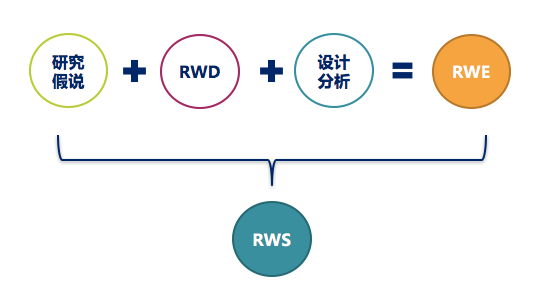
梅斯医访谈 | FDA真实世界证据框架
梅斯医访谈(MedSci Interview, MSI)致力于分享医学专业知识,传播医学前沿观念。
MedSci原创 - FDA,真实世界研究 - 2018-12-12
美国的疫苗安全是如何监管的?
导言最近寨卡病毒感染病例已经在包括美国在内的全球30余个国家被诊断,昨天(2月1日),在美国被证实寨卡病毒可以通过性传播,这更增加了该病毒的危险性。
美中药源 - 疫苗,安全,疫苗监管 - 2018-07-22
FDA审查诺华新型血液肿瘤药物
FDA肿瘤药物咨询委员会在11月06日召开了会议并提前发布了文件,该机构官员没有给出多少评论,而是注重诺华公司768例3期临床试验的相关数据。
cphi - 血液肿瘤,药物 - 2014-11-11
10条中药标准纳入美国药典
加码欧美市场 据中国工程院院士、中国中医科学院院长张伯礼介绍,今年上半年,我国有3个品种进入FDAⅢ期临床试验:天士力生产的复方丹参滴丸已进入病例募集阶段;绿叶制药生产的血脂康胶囊去年完成Ⅱ期临床试验
医药经济报 - 中药标准,美国药典 - 2014-09-04
FDA新冠疫情下临床试验开展指南
新冠疫情流行期间,FDA(美国食药品监督局)和EMA (欧洲药品管理局)分别于3月18号和3月20日各自发布了“在COVID-19大流行期间的临床试验应对指南”
FDA - 2020-03-28
为您找到相关结果约500个