European Radiology:MRI对良、恶性椎体压缩骨折的深度学习评估
2024-02-20 shaosai MedSci原创 发表于上海
机器学习的最新进展允许在放射检查中对各种情况进行敏感、准确和具体的诊断。计算机辅助诊断可以检测VCF并区分良性和恶性骨折椎体。
众所周知,椎体压缩性骨折(VCFs)可导致残疾和生活质量下降。导致VCF的原因包括机械创伤、骨质疏松和肿瘤细胞侵袭。骨质疏松症相关的VCF与年龄增长有关;然而,老龄化的病人也容易患原发性椎体肿瘤或转移。良性和恶性的影像特征在某些情况下是相似的,这两种类型的VCF之间的重叠特征是准确诊断和治疗的主要障碍。
临床上,X线、CT和MRI可单独或联合用于区分良性和恶性VCF。MRI的信号强度和VCF的形状特征是重要标准。在临床实践中,并非所有患者都呈现出典型的良性或恶性VCFs的影像特征。
机器学习的最新进展允许在放射检查中对各种情况进行敏感、准确和具体的诊断。计算机辅助诊断可以检测VCF并区分良性和恶性骨折椎体。一些研究开发了纹理分析和深度学习技术,用于利用基于X线、CT和MRI的成像模式对椎体骨折进行分类。在机器学习的模型设计中,VCF诊断分两步自动处理:识别VCF,然后将其分类为良性或恶性。然而,在每个椎体上进行手动勾画步骤都是半自动的,而且很耗时,在临床日常实践中几乎没有使用。
最近,有研究开发了一种双流对比网络(TSCCN)的深度学习方法来自动检测和分类VCF。尽管如此,TSCCN模型尚未在临床上得到验证。

近日,发表在European Radiology杂志上的一篇研究探讨并验证了成熟TSCCN模型区分VCF的有效性及价值,并比较了模型的性能和本机构放射科医生的评估。
本项研究在123个良性和86个恶性VCF中测试了一个深度学习系统,并使用中位矢状面T1加权图像(T1WI)、带脂肪抑制的T2加权图像(T2WI-FS)以及两者的组合(此后为T1WI/T2WI-FS)来验证TSCCN。同时,分析了接收器操作特征(ROC)曲线以评估TSCCN的性能。计算了TSCCN区分良性和恶性VCF的准确性、敏感性和特异性,并与放射科医生的评估进行比较。测试了类内相关系数(ICCs),以了解放射科医生在区分恶性和良性VCF方面的观察者内部和之间的一致性。
根据T1WI、T2WI-FS和T1WI/T2WI-FS图像得出的TSCCN的ROC图的AUC分别为99.2%、91.7%和98.2%。基于TSCCN的T1W、T2WI-FS和T1W/T2WI-FS的准确率分别为95.2%、90.4%和96.2%,高于放射科医生的准确率。此外,基于TSCCN的T1W、T2WI-FS和T1W/T2WI-FS的特异性也高于放射科医生达到的98.4%、94.3%和99.2%。放射科医生的观察者内和观察者间一致性为:T1WI为0.79-0.85和0.79-0.80,T2WI-FS为0.65-0.72和0.70-0.74,而T1WI/T2WI-FS为0.83-0.88和0.83-0.84。
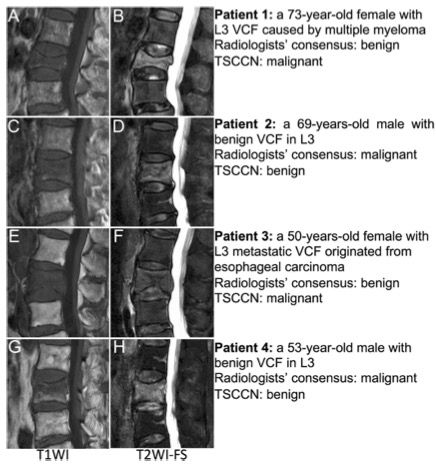
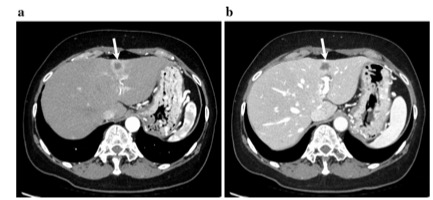
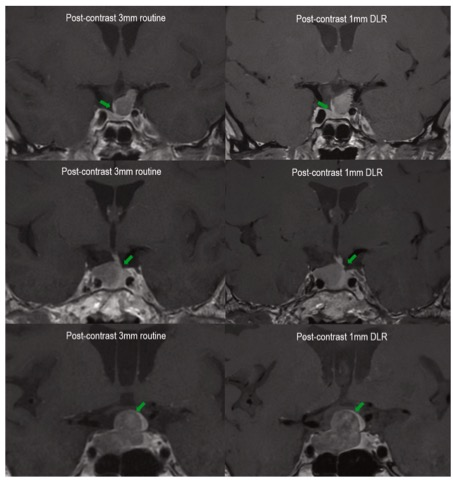
图 TSCCN和放射科医生的假阳性或阴性示例
本项研究包膜,在自动识别良性或恶性VCF方面,TSCCN模型显示出比放射科医生更好的诊断性能,是未来临床应用的一个潜在的、具有临床价值的影像学工具。
原文出处:
Beibei Liu,Yuchen Jin,Shixiang Feng,et al.Benign vs malignant vertebral compression fractures with MRI: a comparison between automatic deep learning network and radiologist's assessment.DOI:10.1007/s00330-023-09713-x
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#深度学习# #椎体压缩骨折#
30