Immunity: 浙江大学史鹏团队揭示小胶质细胞调控外周血压的分子机制
2022-07-23 周科 “神经周K”公众号
小胶质细胞作为大脑免疫系统的重要组成部分,除了发挥免疫监视的作用以外,还可以通过清除细胞碎片、吞噬突触、分泌营养因子维持神经元功能。
小胶质细胞作为大脑免疫系统的重要组成部分,除了发挥免疫监视的作用以外,还可以通过清除细胞碎片、吞噬突触、分泌营养因子维持神经元功能。
高血压是一个重要的全球健康问题。尽管高血压的病因各不相同,但大多数原发性高血压患者存在交感神经活动(SNA)升高,这加剧血压升高,而在去肾交感神经支配后可降低血压。
下丘脑室旁核(PVN)是位于第三脑室附近,可控制交感神经输出。投射到脑干延髓前外侧 (RVLM) 的 PVN 前交感神经元(后续简称PVN-RVLM神经元)功能障碍会引起高血压和肥胖症。

2022年7月21日浙江大学医学院史鹏研究团队揭示了小胶质细胞调节外周血压的机制:小胶质细胞配体(血小板衍生生长因子)-神经元受体(血小板衍生生长因子受体)的互作模式。
1 敲除小胶质细胞血压升高,钾离子电流障碍
研究人员通过基因工具小鼠特异性敲除小胶质细胞后小鼠外周血清去甲肾上腺素(NE)和肾上腺素升高,表明交感神经过度激活。此外,小鼠基础心率增加,收缩动脉压明显升高。
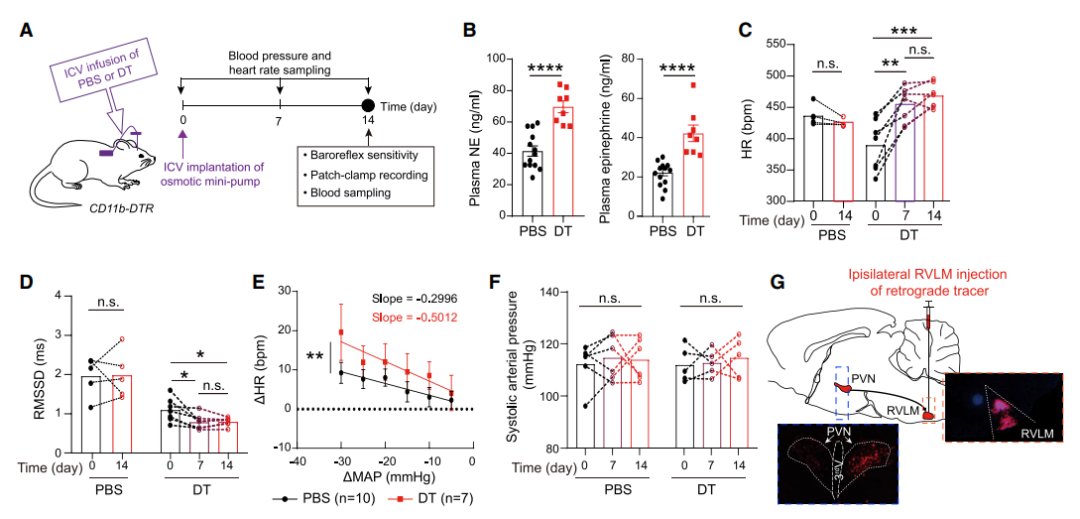
图1:敲除小胶质细胞后小鼠交感神经激活、血压升高
电生理实验发现在正常生理状态下65.4%PVN-RVLM神经元处于不放电状态,剩余进行自发放电活动,但在敲除小胶质细胞后56.9% PVN-RVLM神经元处于放电状态,表明过度兴奋。
在众多离子通道中,钾离子通道是控制产生神经兴奋性的必要因素。在敲除小胶质细胞后低压激活的 A 型钾离子电流和高压激活延迟整流钾离子电流均减弱。单细胞测序技术发现在敲除小胶质细胞后PVN-RVLM神经元编码钾离子通道的基因差异性富集表达,其中Kcnd3基因表达下调较为明显。
选择性抑制Kcnd3基因编码的蛋白Kv4.3可明显阻断低压激活的 A 型钾离子电流,这就表明小胶质细胞可通过表达在神经元上的Kv4.3调控PVN-RVLM神经元放电活动。
2 小胶质细胞来源的PDGF介导钾离子电流障碍
已有研究表明Pdgfb是编码血小板衍生生长因子(PDGF)β亚基的基因可调控少突胶质细胞的钾离子电流,其在小胶质细胞上富集表达,敲除小胶质细胞后Pdgfb表达明显降低。此外,特异性敲除小胶质细胞上的Pdgfb或给与Pdgfb抑制剂可降低Kv4.3在PVN-RVLM神经元上的表达。
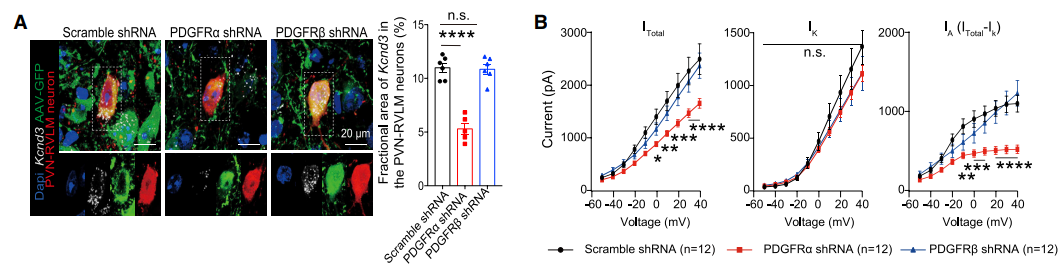
图2:受体PDGFRα 促进Kv4.3蛋白表达
Pdgfb可与两种受体PDGFRα 和PDGFRβ进行结合。离体细胞实验发现PDGFRα拮抗剂可降低小胶质细胞表达Kv4.3,但PDGFRβ拮抗剂则不发挥这种效应。此外,病毒特异性降低PVN-RVLM神经元Pdgfb受体Pdgfbα后能够引起小鼠血压升高,钾离子电流降低,可模拟出敲除小胶质细胞的效应。
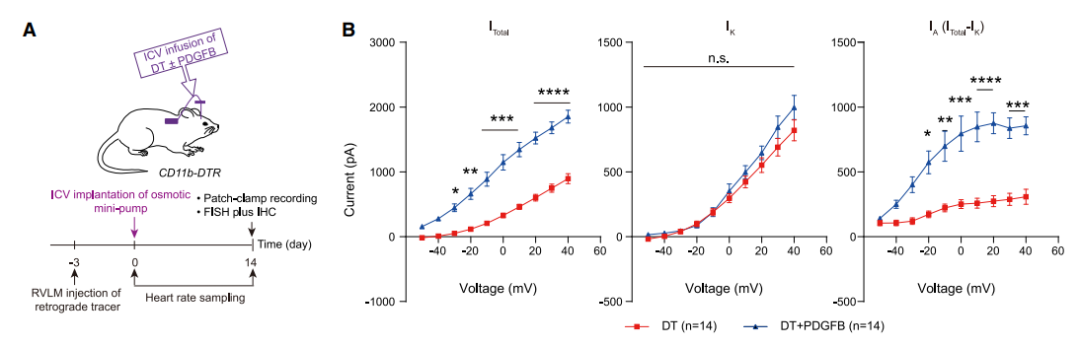
图3:中枢给予Pdgfb可缓解敲除小胶质细胞引起的血压升高
通过侧脑室注射Pdgfb或增加PVN-RVLM神经元Kv4.3表达后能够明显逆转敲除小胶质细胞引起钾离子电流障碍,降低血压。这些结果表明小胶质细胞来源的Pdgfb维持PVN-RVLM神经元钾离子电流。
总的来说,本文揭示了小胶质细胞来源的Pdgfb激活交感神经元的受体PDGFRα促进Kv4.3表达,进而调控钾离子电流介导的交感神经元活性,发挥调节外周血压的功能。
原始出处:
Qianqian Bi, et al. Microglia-derived PDGFB promotes neuronal potassium currents to suppress basal sympathetic tonicity and limit hypertension. Immunity, 2022.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#Immunity#
63
#浙江大学#
57
#胶质细胞#
0
#外周血#
47