Circ Res 中国医科大学赵伟东教授团队发现糖尿病脑微血管病变新靶点
2024-04-11 论道心血管 论道心血管 发表于陕西省
该研究揭示了单核细胞表达的组织蛋白酶D (cathepsin D, CTSD)前体与脑微血管内皮细胞的LRP1(脂蛋白受体相关蛋白1)结合,通过NF-κB通路上调Cav1表达,促进糖尿病微血管病变。
血管功能障碍是2型糖尿病(T2DM)的并发症之一,但T2DM脑微血管病变的确切机制仍不清楚。内皮细胞是血脑屏障的主要成分,其功能可以被循环单核细胞调节,但单核-内皮细胞相互作用与糖尿病血管并发症的关系尚不明确。
2024年3月29日,中国医科大学赵伟东教授团队在Circulation Research上发表了题为“Monocytes Release Pro-Cathepsin D to Drive Blood-to-Brain Transcytosis in Diabetes”的研究论文,揭示了单核细胞表达的组织蛋白酶D (cathepsin D, CTSD)前体与脑微血管内皮细胞的LRP1(脂蛋白受体相关蛋白1)结合,通过NF-κB通路上调Cav1表达,促进糖尿病微血管病变。

首先,研究者通过测序发现CTSD在T2DM尤其合并微血管病变患者的单核细胞中表达增加。构建单核细胞表达人CTSD的转基因小鼠(hCTSDhi)发现,小鼠脑血管通透性增加和神经元损失,导致认知功能障碍。通过透射电镜发现,hCTSDhi小鼠脑内皮中的细胞质囊泡显著增加,表明囊泡介导的胞饮作用增强。
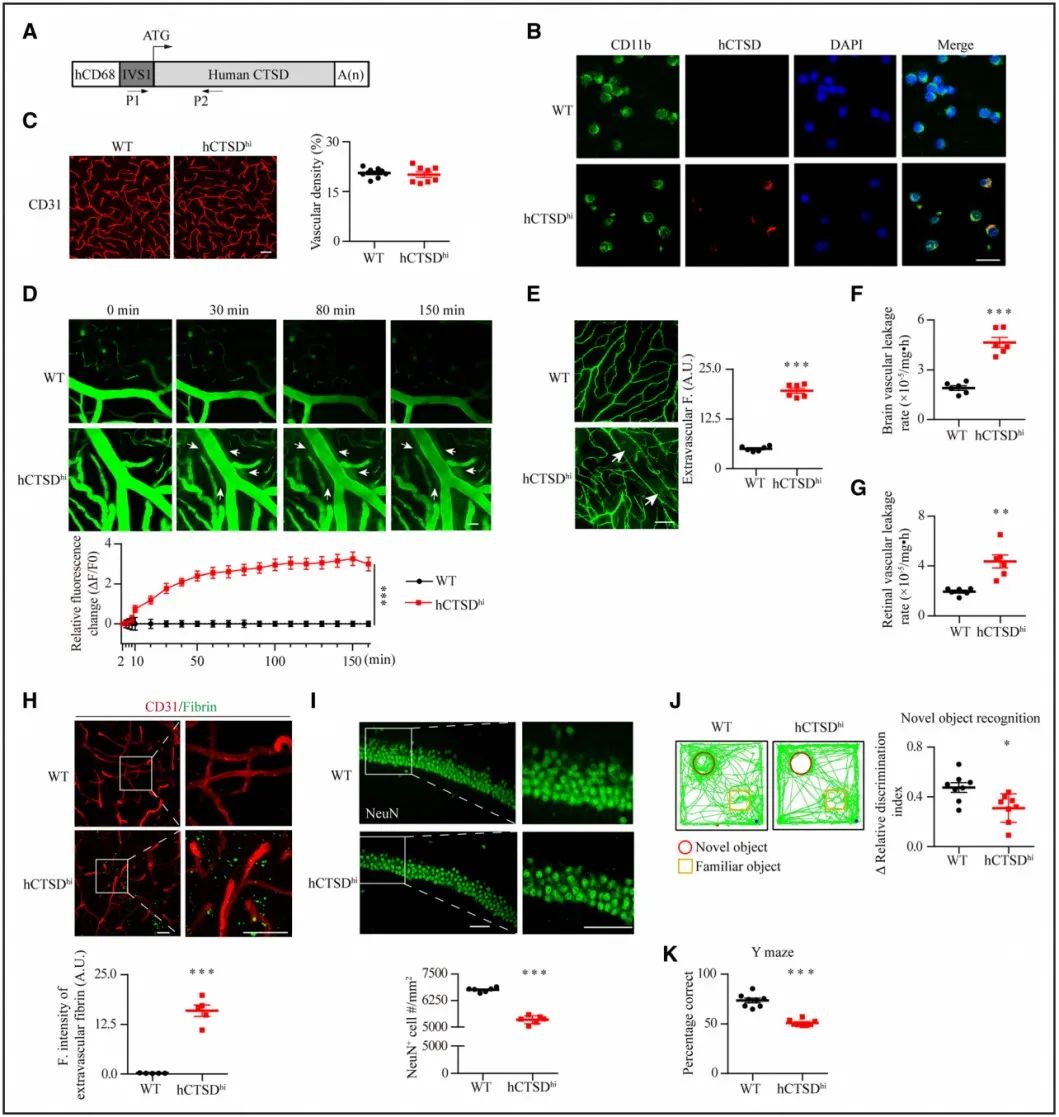
研究者通过单细胞测序、基因富集等实验证实,hCTSDhi小鼠内皮细胞中Cav1表达上调,并且在hCTSDhi小鼠内皮细胞中敲低Cav1可以降低脑血管通透性和细胞质囊泡。进一步研究发现,高糖可刺激单核细胞分泌CTSD前体(proCTSD),proCTSD引起人脑微血管内皮细胞(HBMEC)中Cav1表达增加,胞吞作用增强。
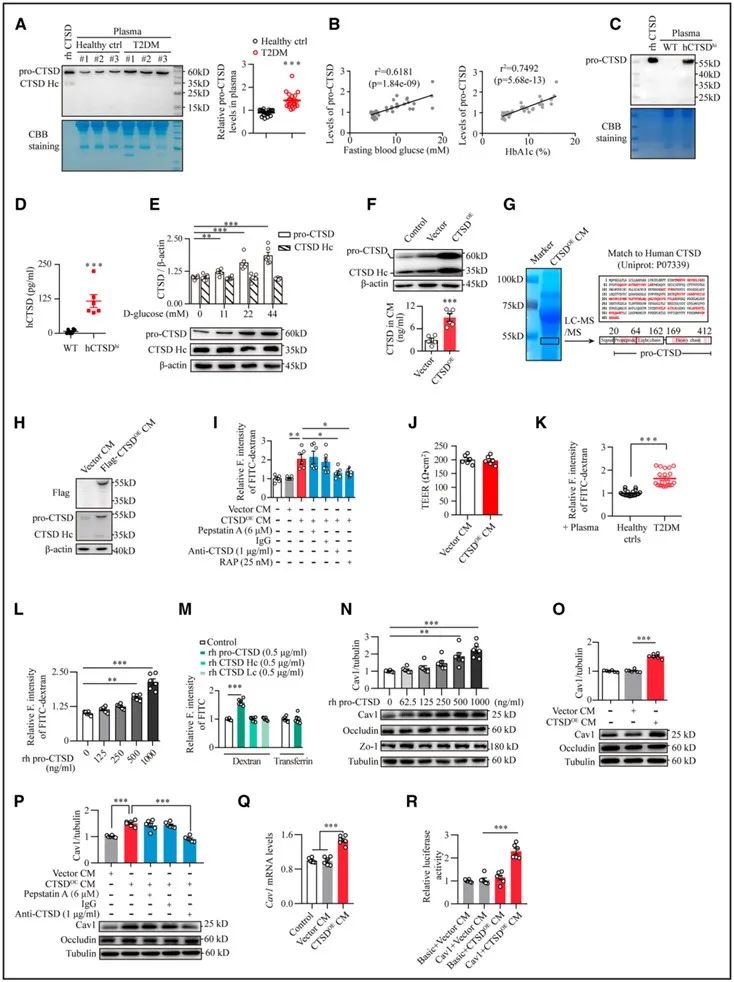
质谱分析和免疫共沉淀等结果表明,proCTSD与内皮细胞LRP1的胞外结构域结合,通过NF-κB通路上调Cav1表达。最后,研究者通过构建单核细胞特异性CTSD敲除小鼠发现,单核细胞中CTSD缺失可逆转糖尿病小鼠脑微血管通透性增加和认知损害。
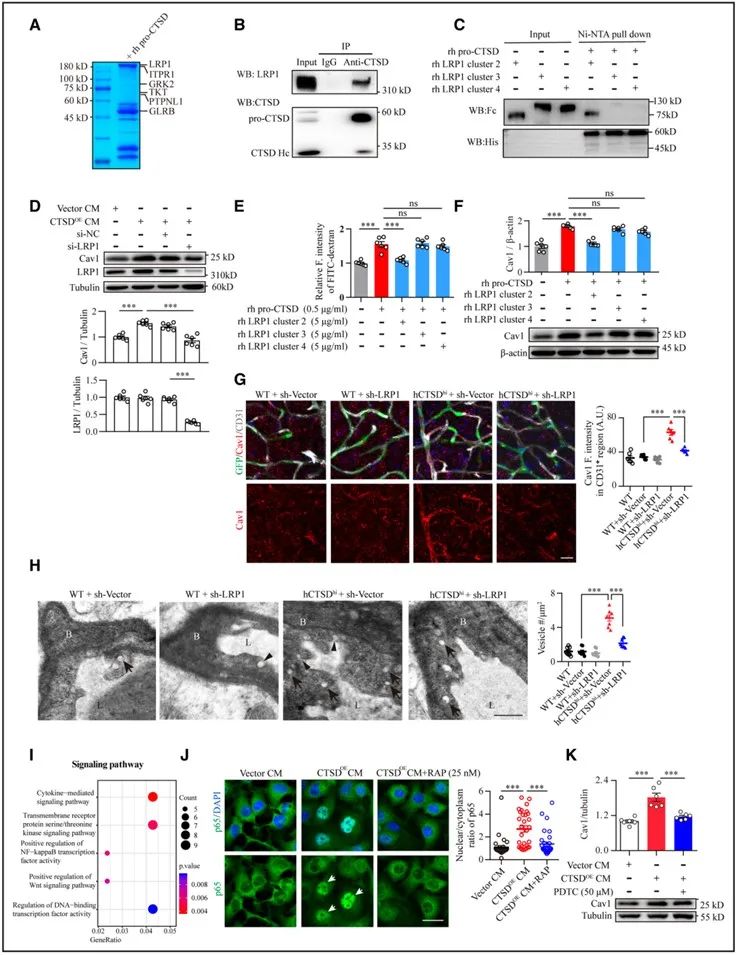
综上所述,本研究揭示了单核细胞表达的CTSD在糖尿病脑微血管病变发病机制中的重要作用,提示单核细胞CTSD可能是糖尿病微血管并发症干预的潜在靶点。
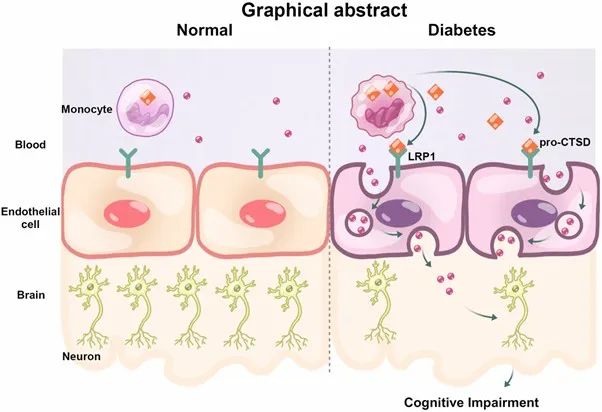
原文链接:
https://doi.org/10.1161/CIRCRESAHA.123.323622
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#脑微血管内皮细胞# #糖尿病脑微血管病# #组织蛋白酶D#
10