Circ Res:iPS技术制作出工程化心脏,心脏移植手术或将不必等待供体配型
2016-03-23 生物谷 生物谷
(图片摘自www.sciecnealert.com) 器官移植手术对于器官衰竭的患者来说是无价的疗法,但是器官短缺,等待人数过多以及昂贵的降低免疫排斥反应的药物等等因素大大地增加了器官移植的困难。 不过,如果有一种新的方法可以不依赖于供体(活人)完整、鲜活的器官而能够同样进行器官移植的话,这一手术的难度是否会降低呢?最近,美国科学家们在这方面做出了突破性的贡献。他们通过体外再生“功能性的

(图片摘自www.sciecnealert.com)
器官移植手术对于器官衰竭的患者来说是无价的疗法,但是器官短缺,等待人数过多以及昂贵的降低免疫排斥反应的药物等等因素大大地增加了器官移植的困难。
不过,如果有一种新的方法可以不依赖于供体(活人)完整、鲜活的器官而能够同样进行器官移植的话,这一手术的难度是否会降低呢?最近,美国科学家们在这方面做出了突破性的贡献。他们通过体外再生“功能性的人体心肌细胞”的方法创造出了工程化的人类心脏。利用这一技术,虽然我们仍然需要一个供体的器官,但是可以与受体的细胞进行融合。
这一技术需要利用“拆包”心脏重新培育出一个完整的心脏——即,将供体来源的活细胞与从受体分离培养得到的iPSC细胞分化出的心脏组织有机地结合在一起。这一步能够将供体器官中能够引发免疫反应的分子去除,代之以受体内的心肌细胞。
“长期以来,心脏再生都是我们的目标,我们目前通过生物工程的方法制作出了功能性的心脏,这能够作为代替性器官给心脏衰竭患者进行移植。”来自麻省总医院再生医学中心的研究员Jacques Guyette说道。
相关结果发表在最近一期的《Circulation Research》杂志上。
“培养出功能性的心脏组织需要克服一系列的困难”,Guyette说道:“这包括提供一个能够支持心脏功能的支架,一群分化除特殊功能的心脏细胞以及适宜细胞生存与发挥功能的环境”。
在该研究中,研究者们共收集到了73颗人类心脏,同时利用IPS技术分化得到5亿个心肌细胞,之后将它们种植到了“拆包”的心脏组织中。
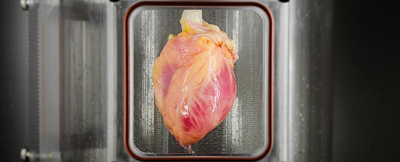
经过一段时间的体外培养,从心肌细胞分化出了较为完整的心脏。这是第一次利用IPS细胞培养出心脏的成功案例。培养好的心脏器官存放在自动生物反应系统(如图所示)中。该系统能够提供足够的营养以及类比生理条件下心脏器官的环境。
希望这一技术能够早日应用于临床治疗,这将是广大亟待心脏移植患者的福音。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#供体#
32
#iPS#
25
厉害
110
好东西啊
75