【论著】| 上海市癌症患者化疗所致恶心呕吐的横断面研究
2024-01-08 中国癌症杂志 中国癌症杂志 发表于陕西省
本研究评估了2022年上海市主要三甲医院CINV的发生情况和处理方式,并探讨CINV相关危险因素,以期进一步改善CINV管理。
[摘要] 背景与目的:化疗所致恶心呕吐(chemotherapy-induced nausea and vomiting,CINV)可使癌症患者机体功能紊乱,甚至导致死亡。预防CINV对于接受致吐性化疗方案的患者至关重要。本研究旨在分析上海市三甲医院CINV的发生情况及处理方式,探讨与CINV相关的危险因素,以期进一步改善CINV管理。方法:选取2022年10月—2022年12月在上海市16家三甲医院接受治疗的376例癌症患者作为研究对象,采用问卷调查的方式开展横断面研究。使用单因素和多因素logistic回归模型分析CINV的影响因素。结果:2022年上海市CINV管理与指南符合率较5年前有显著改善。对于接受高致吐风险化疗方案的患者,指南符合率从21.6%提升至67.0%。对于接受中致吐风险化疗方案的患者,神经激肽-1(neurokinin-1,NK-1)受体抑制剂的使用并不能显著降低CINV的发生率。多因素分析显示,化疗方案是CINV发生的唯一独立危险因素(P<0.05)。结论:化疗方案是影响CINV发生的独立危险因素,临床实践中应优先关注药物本身的致吐风险,做好风险评估,严格遵循指南,从而最大化地控制CINV。
[关键词] 化疗所致恶心呕吐;癌症;横断面研究
[Abstract] Background and purpose: Chemotherapy-induced nausea and vomiting (CINV) can cause severe damage to body functions and even lead to death. The prevention of CINV is critically important in patients receiving emetogenic chemotherapy regimen. This study aimed to investigate the prevalence and treatment of CINV in Grade-A tertiary hospitals in Shanghai and explore risk factors of CINV to improve its management. Methods: The clinical data of 376 cancer patients in Grade-A tertiary hospitals in Shanghai from October 2022 to December 2022 were collected retrospectively. The questionnaire was used to conduct a cross-pal study. The univariate and multivariable logistic regression models were used to evaluate the influencing factors of CINV. Results: The management and coincidence of the guideline in 2022 significantly improved compared to five years ago. For patients receiving high-emetic-risk chemotherapy regimen, the coincidence of the guideline increased from 21.6% to 67.0%. For patients receiving moderate-emetic-risk chemotherapy regimen, the neurokinin-1 (NK-1) receptor antagonist was not significantly associated with CINV. Multivariable analysis showed that the chemotherapy regimen was the only risk factor for CINV during the whole period (P<0.05). Conclusion: The chemotherapy regimen is the main risk factor for CINV. To control CINV better, clinical practitioners should focus on the intrinsic risk of chemotherapy regimens preferentially, estimate the risk and adhere better to guidelines.
[Key words] Chemotherapy-induced nausea and vomiting; Cancer; Cross-pal study
癌症是全球性的公共卫生问题,化疗是其主要治疗方法之一,但也会导致一系列不良反应,如化疗所致恶心呕吐(chemotherapy-induced nausea and vomiting,CINV)等[1]。临床上,最常见的类型是急性和延迟性CINV。急性CINV发生在化疗后数分钟至数小时内,常在24 h内缓解,其高峰通常持续5~6 h。延迟性CINV发生在化疗24 h后,可持续6~7 d[2]。CINV不仅会导致电解质紊乱和营养不良等问题,还会增加患者的焦虑、抑郁等负面情绪,降低患者对治疗的依从性,甚至导致治疗中断,危及生命[3]。
预防CINV是癌症患者护理的重要组成部分,临床上往往会根据化疗药物的预期致吐风险设计不同的预防方案[4]。在没有预防的情况下,预计会有超过90%接受高致吐风险化疗(high emetic risk chemotherapy,HEC)方案的患者和30%~90%接受中致吐风险化疗(moderate emetic risk chemotherapy,MEC)方案的患者出现CINV[5]。值得注意的是,CINV的发生率在不同目标人群、地理区域及处方实践中差异很大,从20%至70%不等[6]。随着近几年专家共识及相关指南的发布,大家对CINV的理解逐渐加深,了解CINV管理的现况数据显得尤为重要[7-8]。因此,本研究评估了2022年上海市主要三甲医院CINV的发生情况和处理方式,并探讨CINV相关危险因素,以期进一步改善CINV管理。
1 资料和方法
1.1 研究对象
本研究是一项多中心横断面研究,纳入复旦大学附属肿瘤医院、复旦大学附属华山医院、复旦大学附属华东医院、复旦大学附属中山医院、上海交通大学医学院附属第一人民医院、上海交通大学医学院附属第六人民医院、上海交通大学医学院附属第九人民医院、上海交通大学医学院附属仁济医院、上海交通大学医学院附属瑞金医院、上海交通大学医学院附属新华医院、同济大学附属上海市肺科医院、同济大学附属东方医院、海军军医大学第一附属医院、海军军医大学第二附属医院、上海中医药大学附属上海市中西医结合医院、上海中医药大学附属龙华医院共16家上海市三甲医院作为多中心研究单位。采用横断面研究样本量估算公式n=t2PQ/d2,公式中n代表样本量,统计学t值为1.96(α取0.05时的固定值),P为预期的患病率,Q=1-P,d为容许误差(设定d为0.05)。2021年发表的一篇中国前期横断面研究[9]共纳入中国四川省17个癌症中心即将接受致吐性化疗方案的1 139例肿瘤患者,最终总体CINV发生率为83%。按照公式计算至少需要样本量约217例。因此,本研究共纳入2022年10月—2022年12月在上述16家上海市三甲医院接受化疗的376例患者。患者纳入标准:① 病理学诊断为癌;② 年满18岁;③ 接受轻微/低致吐风险化疗方案、MEC方案或HEC方案;④ 血液学、肝功能、肾功能等重要器官检查合格。排除标准:① 同时接受化疗和放疗;② 存在认知或沟通障碍;③ 有其他可能导致恶心呕吐的疾病(如肠梗阻和怀孕);④ 癌症疼痛尚未稳定,需要使用阿片类止痛药的患者,或阿片类药物消化道反应未完全控制的患者;⑤ 长期接受皮质类固醇的患者。
1.2 调研工具
根据癌症支持疗法多国学会(Multinational Association of Supportive Care in Cancer,MASCC)指南[7]的CINV评估工具,急性CINV定义为24 h内呕吐发作的累积次数≥1或恶心水平>3,延迟性CINV的定义是2~5天内的累积呕吐发作次数≥1或恶心水平>3[10]。根据研究目的设计资料收集表,采用“问卷星”网站形成工具链接,内容包括年龄、性别、癌种、化疗方案、化疗周期及止吐方案。化疗方案根据抗肿瘤药物的致吐风险分为轻微/低致吐风险化疗方案、MEC方案和MEC方案[11]。化疗周期定义为发生CINV时,患者所处的化疗周期数。止吐方案包括四联方案[5-HT3RA+地塞米松+神经激肽-1(neurokinin-1,NK-1)RA+奥氮平]、三联方案(5-HT3RA+地塞米松+NK-1 RA/奥氮平)、二联方案(5-HT3RA+地塞米松)、单药治疗(5-HT3RA/地塞米松)和无预防用药。
1.3 质量控制
成立多中心调研质量控制微信群,由各参研医院派出1名调研负责人加入微信群,组成质控组,负责对本单位调研质量进行监控和管理。
1.4 统计学处理
采用SPSS 24.0软件对数据进行统计学分析。运用χ2检验分析NK-1受体抑制剂对接受MEC方案患者的止吐效果。采用logistic回归分析对CINV的影响因素进行单因素分析。为降低与结果相关性较弱的单个因素在组合时可能会产生显著影响的可能,本研究以α=0.2为检验水准,允许纳入更多因素进行多因素logistic回归分析。P<0.05为差异有统计学意义。
2 结 果
2.1 研究对象的基本信息
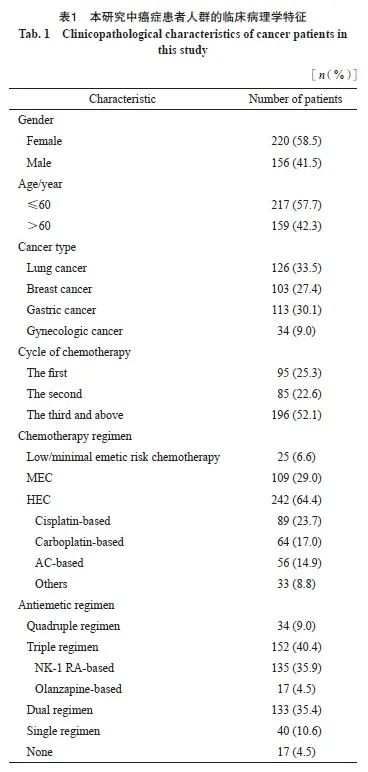
共纳入癌症患者376例,患者纳入流程图见图1。性别、年龄、癌种、化疗所处周期、化疗方案及止吐方案等见表1。其中,男性占41.5%,女性占58.5%,60岁以上的患者占42.3%。原发性肿瘤前3位依次为肺部肿瘤(33.5%)、消化道肿瘤(30.1%)和乳腺肿瘤(27.4%)。242例(64.4%)患者接受HEC方案,109例(29.0%)患者接受MEC方案,25例(6.6%)患者接受轻微/低致吐风险化疗方案。截至2022年12月31日,47.9%的患者正处在第1或第2周期化疗中。分别有40.4%和35.4%的患者选择了三联和二联止吐方案,选择四联止吐方案的患者仅占9.0%。

图1 患者纳入流程图
Fig. 1 Flow chart of patient selection
2.2 CINV的发生情况
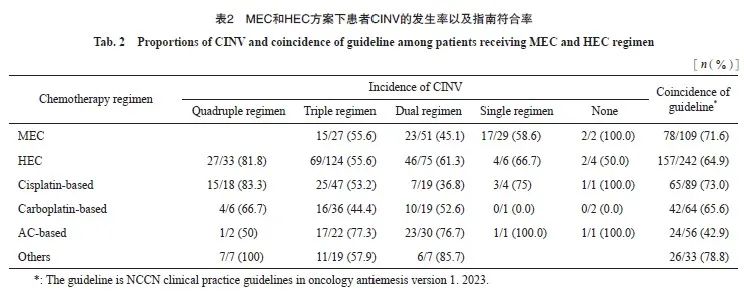
参照2023年美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)指南V1版本[11],使用含AC方案的患者止吐指南符合率最低,仅42.9%。值得注意的是,这部分患者的CINV发生率在所有HEC方案中也是最高的,达76.8%。使用含顺铂和含卡铂方案的患者指南符合率较好,分别为73.0%和65.6%,其CINV发生率也相对较低,分别为57.3%和46.9%。对于MEC方案,指南允许使用二联或三联方案,因而其指南符合率也较HEC方案相对更高(71.6% vs 64.9%),CINV发生率相对更低(52.3% vs 61.25%)。本次横断面研究显示,2022年上海市三甲医院CINV指南符合率为67.0%(表2)。
2.3 NK-1受体抑制剂的止吐效果评价
将接受MEC方案的患者分为使用NK-1受体抑制剂和不使用NK-1受体抑制剂两组,对两组患者的CINV发生情况进行统计学分析。结果显示,NK-1受体抑制剂在接受MEC方案的患者中并未观察到显著的止吐效果差异(χ2=0.510,P>0.05,图2)。
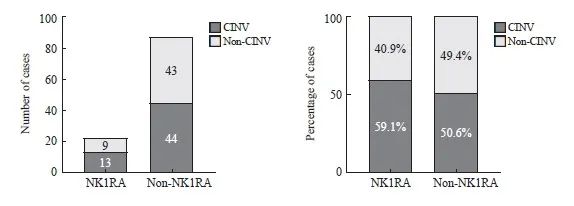
图2 比较接受MEC方案的患者中NK-1受体抑制剂对止吐效果的影响
Fig. 2 Comparison of the effects of NK-1 receptor inhibitors on antiemetic efficacy in patients receiving MEC regimen
2.4 CINV的危险因素分析
2.4.1 急性CINV的危险因素分析
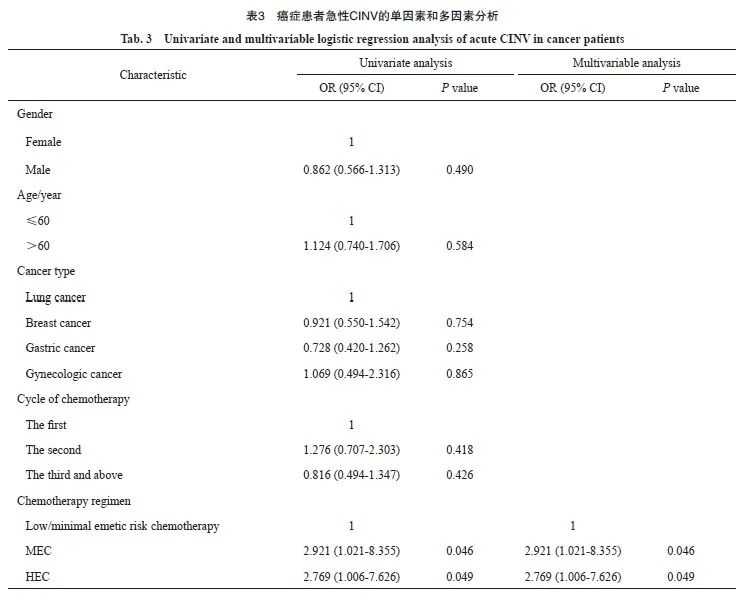
对急性CINV进行单因素和多因素logistic模型分析表明,有且只有化疗方案可能是导致癌症患者发生急性CINV的独立危险因素(P<0.05,表3),而性别、年龄、癌种及化疗周期并不影响CINV的发生(P>0.05)。
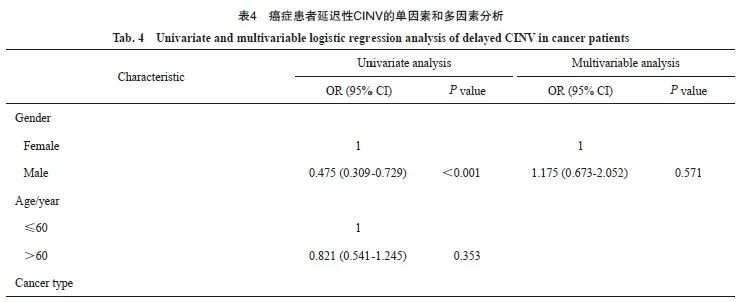
2.4.2 延迟性CINV的危险因素分析
对延迟性CINV进行单因素logistic模型分析表明,性别、癌种及HEC方案可能是导致癌症患者发生延迟性CINV的危险因素(P<0.05),而年龄、化疗周期并不影响CINV的发生(P>0.05)。将单因素logistic模型分析中P<0.20的因素纳入多因素logistic模型分析。结果显示,癌种及HEC方案仍然是延迟性CINV的独立危险因素(P<0.05,表4)。
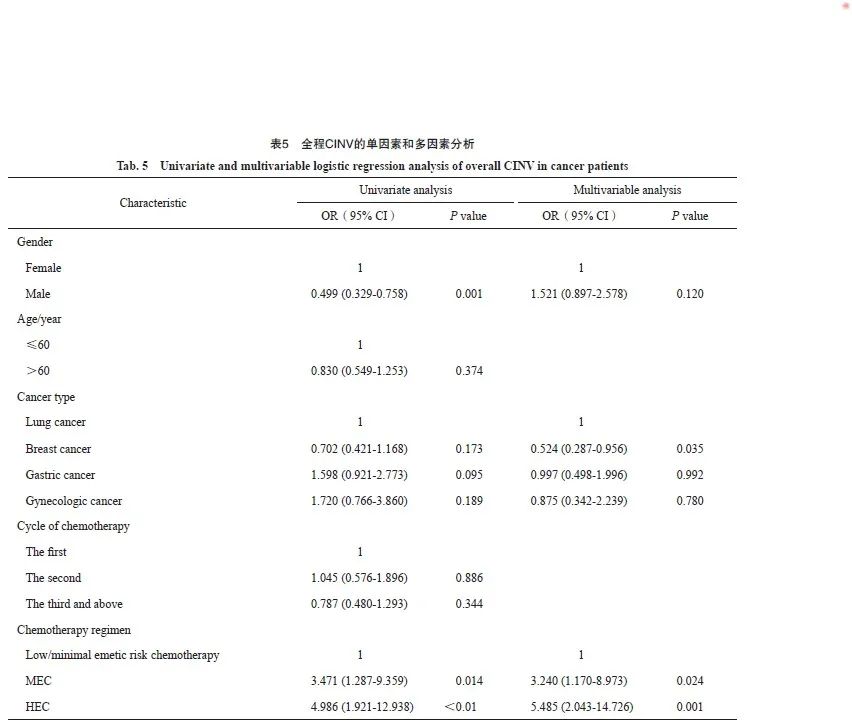
2.4.3 全程CINV的危险因素分析
对全程CINV进行单因素logistic模型分析表明,性别及化疗方案可能是导致癌症患者发生CINV的危险因素(P<0.05),而年龄、癌种及化疗周期并不影响CINV的发生(P>0.05)。将单因素logistic模型分析中P<0.20的因素纳入多因素logistic模型分析。结果显示,癌种及化疗方案是全程CINV的独立危险因素(P<0.05,表5)。

3 讨 论
癌症患者在治疗过程中会出现许多不良反应,其中CINV是化疗引起的常见不良反应之一。国内外肿瘤相关学术协会不仅制定了CINV的相关指南,还倡导及早实施预防给药。临床研究[12-13]表明,使用标准化的预防性止吐可以保护超过70%的患者在风险阶段免受CINV的侵害。由于药物可及性、医师决策的指南一致性和患者依从性等问题,CINV的真实情况远比临床研究结果复杂得多,因此通过真实世界研究进一步分析CINV很有必要。
参考2017版NCCN指南V2版本[14],海军军医大学附属长海医院2016—2017年的一项回顾性研究[15]表明,在使用HEC方案的患者人群中,指南符合率仅21.6%。随着近几年专家共识及相关指南的出台,大家对于CINV的理解逐渐加深[7-8]。本研究再次调研发现,参照2023年NCCN指南V1版本[11],在上海接受HEC方案的患者中,指南符合率达到了67.0%,较5年前获得了显著提升。
2023年NCCN指南V1版本[11]中,接受MEC方案的患者推荐在使用5-HT3受体拮抗剂+地塞米松的基础上联合或不联合NK-1受体抑制剂。既往部分循证医学证据[16]显示,添加NK-1受体抑制剂对于某些特定人群是存在获益的。本次真实世界研究中,NK-1受体抑制剂并未在二联止吐方案的基础上获得额外的止吐效果。因此我们认为二联止吐方案的基础上增减NK-1受体抑制剂都可以作为临床实践中的合理选择,也期待未来有设计良好的随机对照研究可以明确添加NK-1受体抑制剂的获益人群。
最后,本研究对CINV的影响因素进行了单因素和多因素分析,发现癌种是延迟性CINV和全程CINV的危险因素,这与先前的研究结果一致。妇科肿瘤的发病群体是女性,此前研究[17]表明,女性较男性更容易发生CINV,尤其是孕期经历呕吐的妇女。此外,消化道病变本身易发生呕吐,因此消化道肿瘤的CINV发生风险也相对更高。值得注意的是,化疗方案不仅显著影响延迟性CINV和全程CINV,同时是急性CINV的独立危险因素。与轻微/低致吐风险化疗方案相比,采用HEC方案和MEC方案的患者具有更高的CINV发生风险,表明药物本身的致吐风险足以在短期内影响CINV的发生。
本研究探究了2022年上海市CINV的发生情况、处理方式及危险因素,但是由于工作条件的限制,仍存在以下的局限性:① 本次横断面研究仅概述了上海市部分三甲医院的止吐处方模式,仍需更大规模的研究来评估其他地区的止吐模式;② 部分患者的CINV数据仍在随访中,本研究暂时无法对患者预防性止吐用药的后续效果进行有效评价。
综上所述,本研究提示化疗方案作为CINV可能是最重要的独立危险因素,临床实践中应着重关注药物或方案本身的致吐风险,做好风险评估,严格遵循指南,从而最大化地控制CINV。
利益冲突声明:所有作者均声明不存在利益冲突。
[参考文献]
[1]JORDAN K, JAHN F, AAPRO M. Recent developments in the prevention of chemotherapy-induced nausea and vomiting (CINV): a comprehensive review[J]. Ann Oncol, 2015, 26(6): 1081-1090.
[2]LYONS E, LINE C, LEE J J. Developing drugs for prevention of chemotherapy-induced nausea and vomiting: draft guidance from the FDA[J]. Clin Cancer Res, 2021, 27(22): 6072-6074.
[3]GRASSI L, BERARDI M A, RUFFILLI F, et al. Role of psychosocial variables on chemotherapy-induced nausea and vomiting and health-related quality of life among cancer patients: a European study[J]. Psychother Psychosom, 2015, 84(6): 339-347.
[4]NATALE J J. Overview of the prevention and management of CINV[J]. Am J Manag Care, 2018, 24(18 Suppl): S391-S397.
[5]PIECHOTTA V, ADAMS A, HAQUE M, et al. Antiemetics for adults for prevention of nausea and vomiting caused by moderately or highly emetogenic chemotherapy: a network meta-analysis[J]. Cochrane Database Syst Rev, 2021, 11(11): CD012775.
[6]BADARUDIN N S, MOHAMED SHAH N, MOHD KASSIM K N B, et al. A retrospective study on chemotherapy-induced nausea and vomiting in highly/moderately emetogenic chemotherapy: incidence and prescribing practice[J]. Support Care Cancer, 2022, 30(6): 5339-5349.
[7] RAZVI Y, CHAN S, MCFARLANE T, et al. ASCO, NCCN, MASCC/ESMO: a comparison of antiemetic guidelines for the treatment of chemotherapy-induced nausea and vomiting in adult patients[J]. Support Care Cancer, 2019, 27(1): 87-95.
[8] 上海市抗癌协会癌症康复与姑息专业委员会. 化疗所致恶心呕吐全程管理上海专家共识(2018年版)[J]. 中国癌症杂志, 2018, 28(11): 946-960.
Cancer Rehabilitation and Palliative Care Committee of Shanghai Anti-Cancer Association. Shanghai Consensus Guidelines for the Management of chemotherapy-induced nausea and vomiting (2018 edition)[J]. Chin Oncol 2018, 28(11): 946-960.
[9] SUN Y, ZHENG Y Z, YANG X Y, et al. Incidence of chemotherapy-induced nausea and vomiting among cancer patients receiving moderately to highly emetogenic chemotherapy in cancer centers in Sichuan, China[J]. J Cancer Res Clin Oncol, 2021, 147(9): 2701-2708.
[10] COOKSLEY T, GIROTRA M, GINEX P, et al. Multinational Association of Supportive Care in Cancer (MASCC) 2020 clinical practice recommendations for the management of immune checkpoint inhibitor endocrinopathies and the role of advanced practice providers in the management of immunemediated toxicities[J]. Support Care Cancer, 2020, 28(12): 6175-6181.
[11] National Comprehensive Cancer Network. NCCN Guidelines Version 1. 2023 Antiemesis[EB/OL]. (2023-03-23) [2023-08-30]. https://www.nccn.org/guidelines.
[12] HESKETH P J, GRUNBERG S M, GRALLA R J, et al. The oral neurokinin-1 antagonist aprepitant for the prevention of chemotherapy-induced nausea and vomiting: a multinational, randomized, double-blind, placebo-controlled trial in patients receiving high-dose cisplatin--the Aprepitant Protocol 052 Study Group[J]. J Clin Oncol, 2003, 21: 4112-4119.
[13] POLI-BIGELLI S, RODRIGUES-PEREIRA J, CARIDES A D, et al. Addition of the neurokinin 1 receptor antagonist aprepitant to standard antiemetic therapy improves control of chemotherapy-induced nausea and vomiting. Results from a randomized, double-blind, placebo-controlled trial in Latin America[J]. Cancer, 2003, 97: 3090-3098.
[14] BERGER M J, ETTINGER D S, ASTON J, et al. NCCN guidelines insights: antiemesis, version 2. 2017[J]. J Natl Compr Canc Netw, 2017, 15(7): 883-893.
[15] 许 晶,李 洁,张美静, 等. 化疗相关性恶心呕吐的回顾性研究[J]. 临床肿瘤学杂志, 2018, 23(5): 440-443.
XU J, LI J, ZHANG M J, et al. Adherence to NCCN antiemesis guideline for chemotherapy induced nausea and vomiting: a retrospective study in changhai hospital[J]. Chin Clin Oncol, 2018, 23(5):440-443.
[16] ZHANG Y X, YANG Y P, ZHANG Z H, et al. Neurokinin-1 receptor antagonist-based triple regimens in preventing chemotherapy-induced nausea and vomiting: a network metaanalysis[J]. J Natl Cancer Inst, 2017, 109(2): djw217.
[17] SEKINE I, SEGAWA Y, KUBOTA K, et al. Risk factors of chemotherapy-induced nausea and vomiting: index for personalized antiemetic prophylaxis[J]. Cancer Sci, 2013, 104(6): 711-717.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#癌症# #横断面研究# #化疗所致恶心呕吐#
38