【JITC】HDT/ASCT联合CAR-T治疗R/R LBCL再添力证
2024-04-20 聊聊血液 聊聊血液 发表于陕西省
该研究结果为HDT/ASCT联合CAR-T治疗R/R LBCL再添力证,证实治疗适合移植的R/R LBCL患者具有令人印象深刻的疗效,可改善CNCT19的性能,且具有良好的安全性。
ASCT联合CAR-T
CD19 CAR-T细胞治疗是复发或难治性大B细胞淋巴瘤(R/R LBCL)的突破性进展,但仍有大约2/3的患者在CD19 CAR-T细胞治疗后没有反应或复发,导致预后不佳,需要进一步改善CAR-T的疗效。既往研究表明,强化清淋预处理和联合造血干细胞输注可促进过继转移T细胞的扩增,增强抗肿瘤作用。
因此中国医学科学院血液病医院(中国医学科学院血液学研究所)开展了一项I/II期单臂、单中心研究,纳入一线免疫化疗难治性或挽救性化疗后R/R状态且适合移植的LBCL患者,在清髓性大剂量化疗和自体干细胞移植(HDT/ASCT)后给予CNCT19(抗CD19 CAR-T细胞),以评估该联合方案的安全性和有效性;还结合该研究和CNCT19单药治疗R/R LBCL的其他研究,使用冷冻外周血单核细胞样本评估了联合治疗对CNCT19细胞体内性能的影响。
研究结果近日发表于《Journal for ImmunoTherapy of Cancer》,共同通讯作者为邹德慧教授和郑文婷教授。

研究方法
该研究纳入纳入对一线含利妥昔单抗的蒽环类化疗方案难治和/或在至少两个周期的挽救性化疗后处于R/R状态、且适合移植的LBCL患者。单采分两部分:一部分用于采集造血祖细胞HDT/ASCT,一部分采集外周血单核细胞(PBMC)用于制备CNCT19。根据临床医生判断在HDT/ASCT和CNCT19治疗之前给予挽救性或桥接治疗,以实现最佳的疾病控制。在CNCT19产品可用时,给予GBC/M预处理方案(吉西他滨600 mg/m2/小时,以75 mg/m2的负荷输注3小时,-7天至-3天,白消安105 mg/m2-7天至-5天,环磷酰胺45 mg/kg或美法兰60 mg/m2,-3天至-2)。第0天输注自体干细胞,第3天(±1天)输注CNCT19(图1A)。
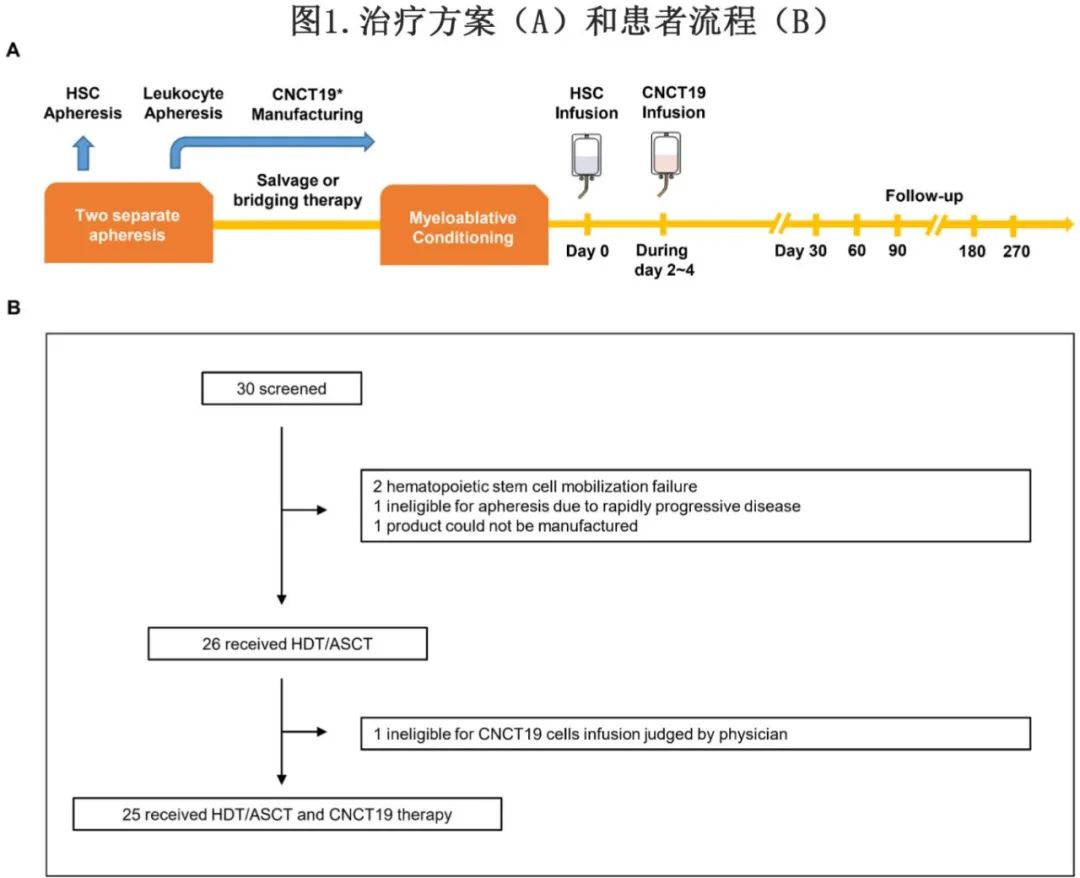
根据TOXicity工作组标准评估细胞因子释放综合征(CRS)和CAR-T细胞相关脑病综合征(CRES)。根据Lugano 2014评估疗效。研究的主要终点为不良事件发生率和最佳总缓解率(ORR,完全缓解[CR]+部分缓解[PR])。次要终点包括CR率、缓解持续时间(DOR)、无病生存期(DFS)、无进展生存期(PFS)和总生存期(OS)。
在CNCT19输注后1、2、4、8后采集PBMC样本进行流式评估。使用该研究和CNCT19治疗R/R LBCL的其他研究中的冷冻样本进行探索性分析,评估联合治疗对CNCT19细胞体内性能的影响。还根据长期缓解状态,评估CNCT19耗竭状态与临床结局的关系。
研究结果
患者特征
共筛选30例患者,最终25例接受HDT/ASCT和CNCT19输注,纳入安全性和疗效分析集(图1B)。
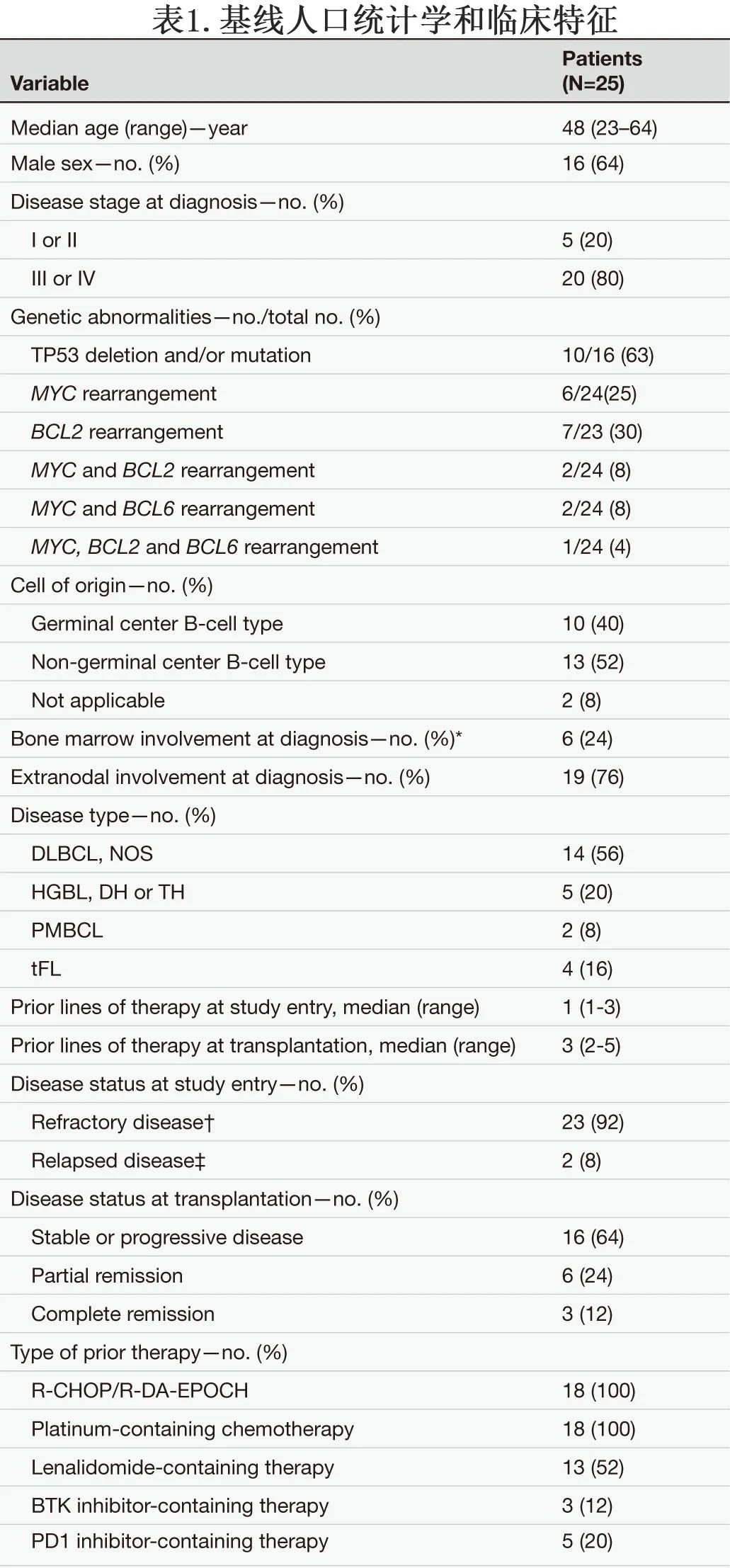
中位年龄为48岁,男性患者占64%。纳入的患者包括:14例(56%)DLBCL,非特指型;5例(20%)伴MYC、BCL2和/或BCL6重排的高级别B细胞淋巴瘤(HGBL);2例(8%)原发性纵隔LBCL;4例(16%)转化滤泡性淋巴瘤。16例患者中有10例(63%)检测到TP53缺失和/或突变。在入组时,23例患者(92%)为难治性疾病,2例为复发性疾病。20例(80%)患者对一线免疫化疗R-CHOP或R-DAEPOCH耐药。入组后,所有患者均接受挽救性或桥接治疗,移植时既往治疗线数中位数为3。16例患者(64%)在移植和CNCT19治疗时仍表现为疾病进展或稳定。表1总结了患者的人口统计学特征。
单采及造血干细胞和CNCT19细胞输注
从PBMC单采或CD34+造血干细胞单采到开始清髓性大剂量化疗的中位时间分别为31天和43天。此外,两次单采之间的中位间隔为18天。移植期间,再输注CD34+造血干细胞的中位数为2.8×106细胞/kg。除1例动员不良患者同时接受外周血和骨髓干细胞输注外,所有患者均只接受外周血干细胞输注。输注CNCT19的中位数为2.0×106/kg。CD34+干细胞与CNCT19输注之间的中位间隔为3天。1例患者因怀疑活动性感染,CNCN19输注延迟至第5天。
安全性
所有患者均发生≥3级不良事件,常见毒性包括细胞减少、疲劳、发热性中性粒细胞减少、腹泻和粘膜炎(表2)。12%的患者发生≥3级转氨酶升高,与GBC/M预处理治疗有关。在整个治疗过程中未观察到非预期毒性或治疗相关死亡。干细胞回输后中性粒细胞和血小板恢复的中位时间分别为10天和16.5天。在CNCT19输注后3个月,8例患者(32%)发生迟发性≥3级血细胞减少,均存在血小板减少,其中3例患者(12%)同时出现中性粒细胞减少。
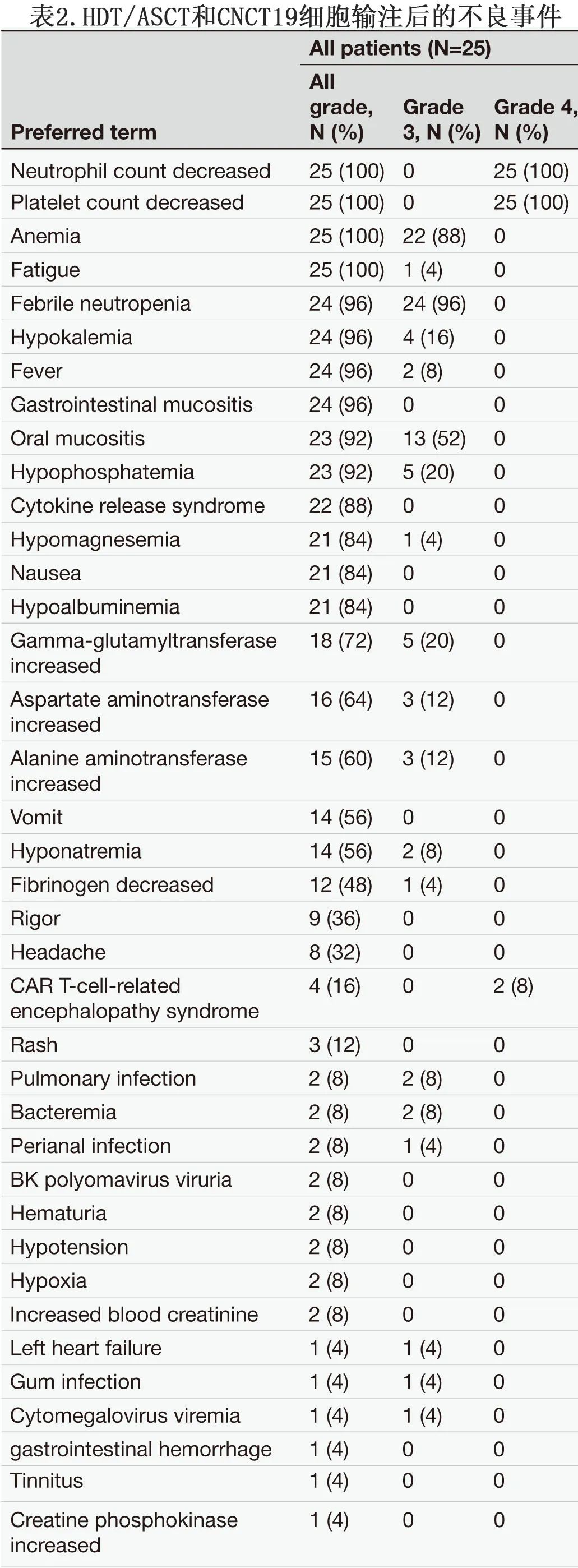
22例患者(88%)发生CRS,均为低级别(1级84%,2级4%;表2)。从CNCT19输注到CRS发作的中位时间为1天,至缓解的中位时间为8天。52%的患者接受托珠单抗、28%的患者接受糖皮质激素治疗CRS。CRS发作与给予托珠单抗和糖皮质激素的中位间隔均为2天。糖皮质激素治疗CRS的中位累积剂量为17.5mg地塞米松当量。4例(16%)患者发生CRES,其中2例为≥3级(表2)。糖皮质激素治疗后,所有CRES完全消退。
疗效
从CNCT19输注到数据截止时,中位随访27.0个月。最佳ORR为92.0%,最佳CR率为72.0%。CNCT19输注后3和6个月,分别有80.0%和72.0%的患者持续缓解(图2)。

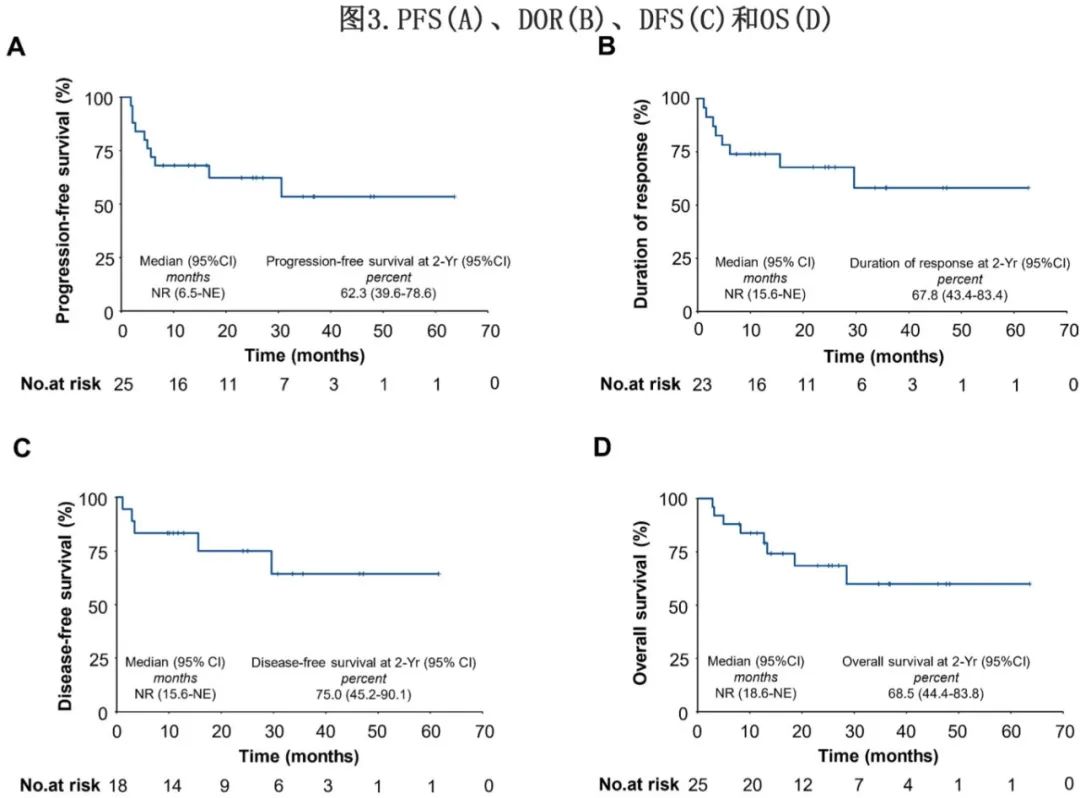
中位PFS、DOR、DFS和OS均未达到,2年PFS、DOR、DFS和OS分别为62.3%、64.9%、75.0%和68.5% (图3)。在CNCT19输注后3个月或6个月持续缓解的患者中,2年PFS分别为77.9%和86.6%。
入组时的疾病状态对联合治疗的反应没有影响,复发和难治性疾病患者的ORR分别为100%和91.3% (p>0.999),CR率分别为100%和69.6% (p>0.999)。移植时接受过≥3线治疗的患者(3L+组,N=14)与接受过2线治疗的患者(2L组,N=11)表现出相似的反应:HDT/ASCT和CNCT19治疗后,2L组和3L+组的ORR分别为100%和85.7% (p=0.487),CR率分别为81.8%和64.3% (p=0.407)。
CNCT19药代动力学
CNCT19水平在注射后10天达到峰值。CNCT19的最大扩增中位数为468个细胞/μL,0-28天的曲线下面积中位数为4499个细胞/μL。2年后,在2例持续CR患者中检测到CNCT19。
联合治疗组和单纯CAR-T组的基线特征对比
在探索性分析中,联合治疗组(HDT/ASCT-CNCT19队列)有13例患者和单纯CNCT19治疗组(CNCT19队列) 有18例患者获得可用的冷冻PBMC样本,可比较两队列中CNCT19在体内的性能。两个队列的患者特征相似,但联合治疗组更年轻(42岁 vs 52岁,p=0.031)、HGBL比例更高(双或三打击)(31% vs 0,p=0.023)、CNCT19输注数量更少(中位数,2×106/kg vs 2.72×106/kg,p=0.002)。
两组输注后的循环CNCT19扩增能力和耗竭状态
在两组(HDT/ASCT-CNCT19和CNCT19) 输注后的第1、2和4周,通过流式细胞术评估外周CNCT19的扩增能力。与CNCT19组相比,HDT/ASCT-CNCT19组患者在2周时CD8+ CAR-T细胞扩增明显更好,无论是比例还是绝对细胞数量(图4A、B)。此外,在1-4周时,HDT/ASCT-CNCT19组的CD4+ CAR-T细胞扩增明显优于CNCT19组(图4C)。两组的CD8+和CD4+ CAR- T细胞扩增无差异(图4A-C)。此外,通过流式细胞术对Ki67(作为细胞增殖指标)进行评估。输注一周后,两组CAR-T细胞的增殖率均达到最高(图4D)。在HDT/ASCT-CNCT19队列中,大多数CD8+和CD4+ CAR-T细胞为Ki67+(分别约为80%和60%),在输注后1周显著优于CNCT19队列(分别约为60%和20%)(图4D)。在两组中,CD8+和CD4+ CAR-T细胞的Ki67+细胞比例在第2周急剧下降至~20%,但第4周CNCT19队列中进一步下降,导致Ki67+细胞与HDT/ASCT-CNCT19队列相比显著较少(图4D)。在两组中,CAR- T细胞均表现出较差的增殖能力(图4E)。
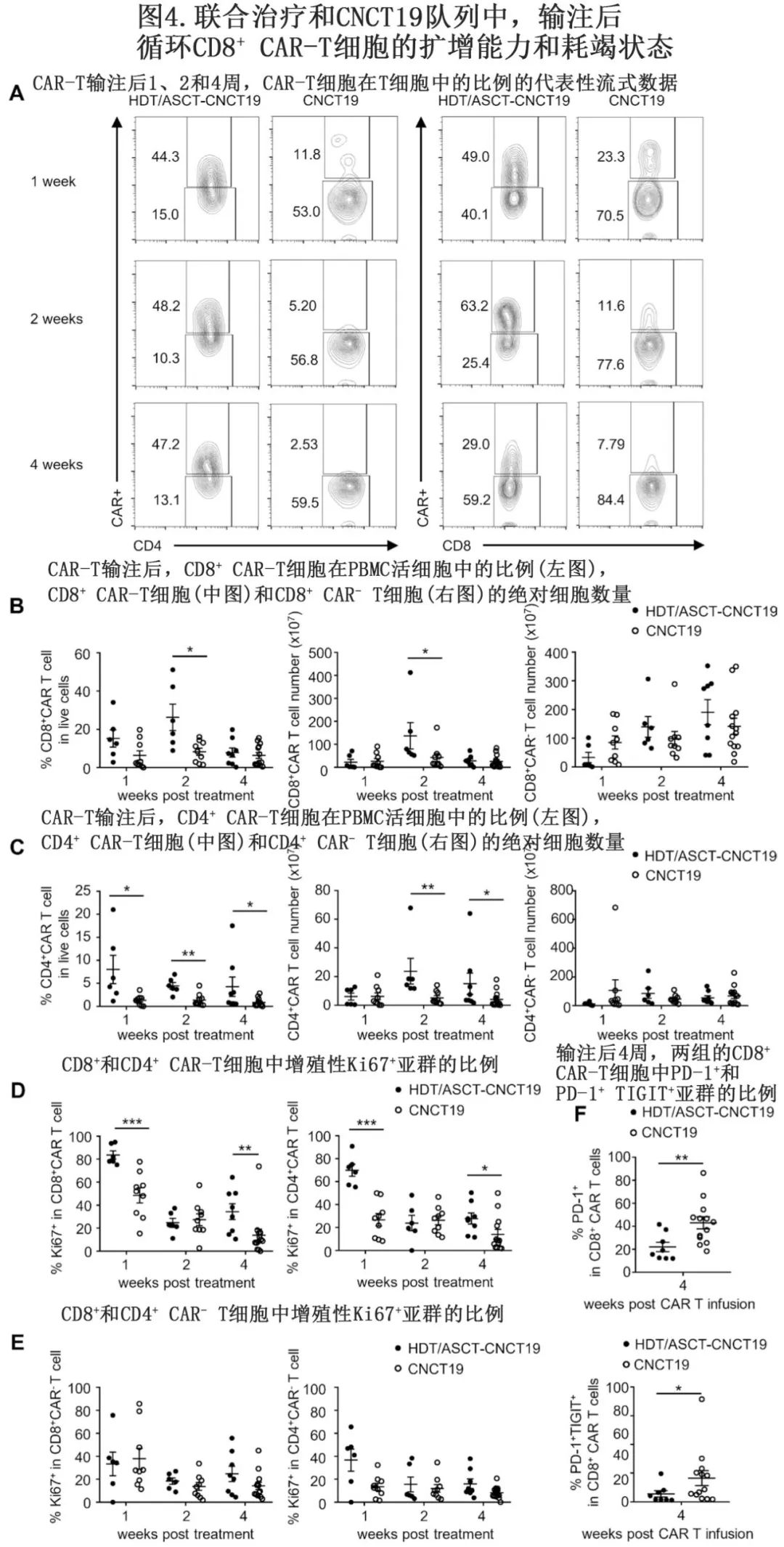
还检测了外周CNCT19的分化状态,因其与过继转移T细胞的细胞毒效应能力密切相关。各组CD8+ CAR-T细胞输注后主要分化为CCR7-CD45RO+ TEM和CCR7-CD45RO- TEMRA亚群。值得注意的是,在输注1周后,HDT/ASCT-CNCT19组CD8+ CAR-T细胞和CD4+ CAR-T细胞中CCR7+CD45RO+ TCM亚群的数量明显少于CNCT19组,而TEM亚群的数量明显多于CNCT19组,表明HDT/ASCT-CNCT19组具有更好的细胞毒效应能力。然而,在HDT/ ASCT-CNCT19队列中,CD8+ CAR- T细胞在1周时含有较少的效应记忆亚群,但有更多的终末分化效应T细胞。两组间CD4+ CAR- T细胞的分化无差异。
还检测了循环CD8+ CAR-T细胞输注后的衰竭状态。如图4F所示,输注后4周,HDT/ASCT-CNCT19队列中CD8+ CAR-T细胞的PD-1+和PD-1+TIGIT+亚群的频率明显低于CNCT19队列。
输注后循环CD8+ CNCT19耗竭状态与患者结局的相关性
作者探讨了输注CNCT19后1-2个月,CD8+ CNCT19中PD1+和/或TIGIT+亚群存在与临床结果的相关性,两组患者合并分析。在CNCT19治疗后1-2个月CR/PR患者中,CD8+ CNCT19中TIGIT+亚群的频率显著低于未缓解(NR)患者,但在复发患者与NR患者没有差异(图5A)。同时,CR/PR患者的CD8+ CNCT19中PD-1+亚群的频率明显低于NR患者和复发患者(图5B)。值得注意的是,CD8+ CNCT19中PD-1+ TIGIT+亚群的频率与各组相关(图5C),NR患者中PD-1+ TIGIT+亚群的频率最高,CR/PR患者中PD-1+ TIGIT+亚群的频率最低。
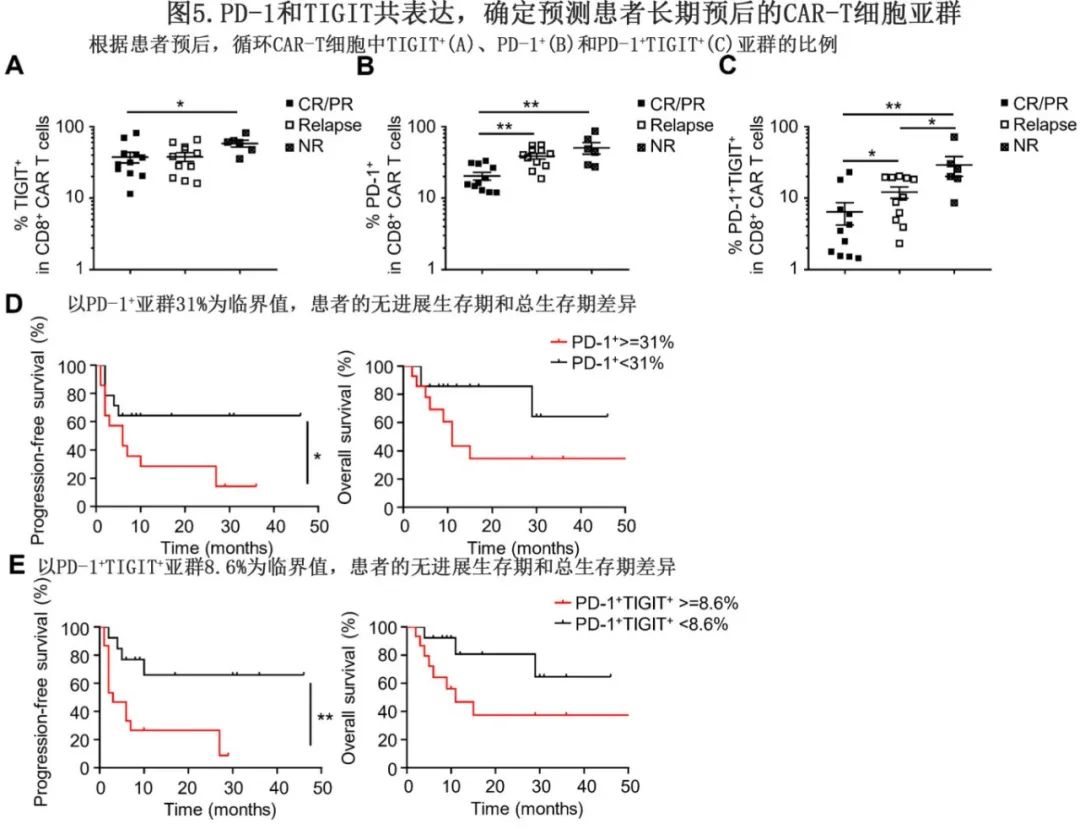
此外,根据两个队列(n=28)中所有患者CD8+ CNCT19中PD1+亚群的中位比例,确定31%为潜在相关值(临界值)。CD8+ CNCT19中PD1+比例<31%的患者(n=14)的PFS明显优于≥31%的患者(n=14, p=0.04)(图5D)。此外,基于两个队列中所有患者的中位数,CD8+ CNCT19中PD1+TIGIT+频率的临界值为8.6%,CD8+ CNCT 19中PD1+TIGIT+比例<8.6%的患者(n=13)的PFS明显优于≥8.6%的患者(n=15, p=0.0053)(图5E)。
总结
该I/II期研究共纳入25例适合移植的R/R LBCL患者,在HDT/ASCT后输注CAR-T细胞,联合治疗的ORR为92.0%,CR率为72.0%;2年PFS率为62.3%,2年OS率为68.5%。未观察到非预期毒性,CRS均为低级别,2例(8%)发生≥3级CAR-T细胞相关脑病综合征。对CNCT19体内行为的比较表明,与接受CNCT19单药治疗的患者相比,联合治疗组患者CNCT19细胞的体内扩增增强,长期耗竭形成减少。
该研究结果为HDT/ASCT联合CAR-T治疗R/R LBCL再添力证,证实治疗适合移植的R/R LBCL患者具有令人印象深刻的疗效,可改善CNCT19的性能,且具有良好的安全性。疗效的改善可能归因于,与CNCT19治疗相比,联合治疗可增强CNCT19的扩增能力,并减少CNCT19输注后的长期耗竭。考虑到该研究的单臂设计和病例数量有限,需要开展随机研究以比较联合治疗与CAR-T细胞治疗,可以为联合治疗的优势提供更有力的证据。
参考文献
Liu W, Zou H, Chen L, et al. Combinational therapy of CAR T-cell and HDT/ASCT demonstrates impressive clinical efficacy and improved CAR T-cell behavior in relapsed/refractory large B-cell lymphoma. Journal for ImmunoTherapy of Cancer 2024;12:e008857. doi:10.1136/ jitc-2024-008857
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#CAR-T# #HDT/ASCT# #R/R LBCL#
12