【Nat Commun】BCMA和CD19双特异性CAR-T治疗RRMM的中国I/II期研究
2024-04-28 聊聊血液 聊聊血液 发表于上海
该研究发现输注 BC19 双特异性 CAR-T 细胞是管理 RRMM 患者的一种可行、安全和有效的策略。
BCMA和CD19 CAR-T
尽管BCMA CAR-T细胞治疗在复发/难治性多发性骨髓瘤(RRMM)中取得了很高的治疗反应,但单靶点免疫治疗存在原发性耐药和复发的问题,解决该问题的方法之一就是使用双靶点CAR-T细胞,例如BCMA/CD38。
在大多数患者中,CD19在小部分骨髓瘤细胞(10.3-80%)上以超低密度表达,CD19low骨髓瘤细胞可以被抗CD19 CAR-T细胞消灭。此外,在大剂量美法仑和挽救性自体造血干细胞移植(Auto-HSCT)后给予抗CD19 CAR-T细胞在RRMM中也显示出一定疗效。基于此,国内学者曾开展前瞻性研究,证明人源化抗CD19和抗BCMA CAR-T细胞联合输注在RRMM患者中是可行的。
国内学者进一步设计了二代双特异性BC19 CAR,包含抗 BCMA 单链可变片段 (scFv) 和人源化抗CD19 scFv,并于近日在《Nature Communications》发表了双特异性 BC19 CAR-T 细胞的临床前结果和 I/II 期研究中治疗RRMM患者的结局。通讯作者为徐州医科大学附属医院曹江教授、郑骏年教授和徐开林教授。

I/II期研究结果
该开放标签、单臂、I/II期研究共筛选了64例患者,其中54例入组,4例患者在输注前因疾病快速进展而退出,最终50例 RRMM 患者接受 BC19 CAR-T 细胞输注。
CAR-T细胞输注后最常见的急性不良事件为血液学毒性和CRS。50例患者均发生血液学不良事件,包括100%的患者中性粒细胞减少症、100%的患者白细胞减少症、94%的患者贫血和88%的患者血小板减少症。3-4级血液学不良事件包括:中性粒细胞减少症(49/50例[98%])、白细胞减少症(48例[96%])、血小板减少症(33例[66%])和贫血(32例[64%])。在接受BC19 CAR-T细胞输注第0天后发生3-4级细胞减少事件的患者中,在第28天恢复到≤2级的比例:白细胞减少(30例[60%])、中性粒细胞减少(27例[54%])、贫血(14例[28%])和血小板减少(8例[16%])。
46例患者(92%)发生CRS, 4例患者8%为≥3级。CRS发作的中位时间为7天,中位持续时间为3天。2例患者(4%)发生1级神经毒性事件,未观察到3-5级神经毒性。6例患者(12%)同时接受托珠单抗和糖皮质激素治疗,19例(38%)患者接受托珠单抗治疗,16例(32%)患者接受糖皮质激素治疗。1例CR患者在2级CRS后第19天出现噬血细胞性淋巴组织细胞症,最终死于感染性休克和胃肠道出血。
除了B细胞再生障碍(aplasia)、低丙球蛋白血症和感染外,晚期不良事件(CAR-T细胞输注后超过3个月)很少。45例患者发生B细胞再生障碍,输注后平均持续时间为138天。CAR-T细胞治疗前20%(10/50)的患者发生低丙球蛋白血症,BC19 CAR-T细胞输注后3个月后51%(23/45)的应答者出现低丙球蛋白血症。49例患者中有14例(29%)在CAR-T细胞输注后超过3个月发生≥3级血细胞减少。
42例(84%)在CAR-T输注后接受G-CSF治疗中性粒细胞减少症。17例(34%)患者因中性粒细胞减少症而接受抗真菌预防治疗,42例(84%)患者接受了抗病毒预防治疗,16例(32%)患者接受抗肺孢子虫预防治疗,随访期间未发现肺孢子虫感染。CAR-T输注后的前三个月有30例(60%)患者发生感染,多为轻中度 (20/30;66.7%)。最常见的微生物为细菌(n=9),其次为真菌(n=3)和病毒(n=1)。在存活超过3个月的49例患者中,19例(39%)在3个月后发生26起感染,其中10例(20%)发生11起重度感染(定义为≥3级)。17例(35%)患者发生肺部感染,1例(2%)患者发生结肠炎。1例(2%)发生带状疱疹,1例(2%)发生菌血症,最终死于菌血症。除1例5级感染外,所有感染均经及时治疗得到控制。
数据截止时,8例患者(16%)在随访期间死亡,4例患者(8%)死于疾病进展或相关并发症。
疗效
46例患者(92%)对BC19 CAR-T细胞达到总体缓解(≥PR),包括18例(36%)sCR,12例(24%)CR, 9例(18%)VGPR和7例(16%)PR,4例(8%)患者SD为最佳缓解。至首次≥PR的中位时间为23.5天,至最佳缓解的中位时间为1.9个月。7例髓外病变患者中有6例(86%)的获得总体缓解。在曾接受过CAR-T细胞治疗的5例患者中,2例达到sCR, 1例达到PR,另外2例为SD。
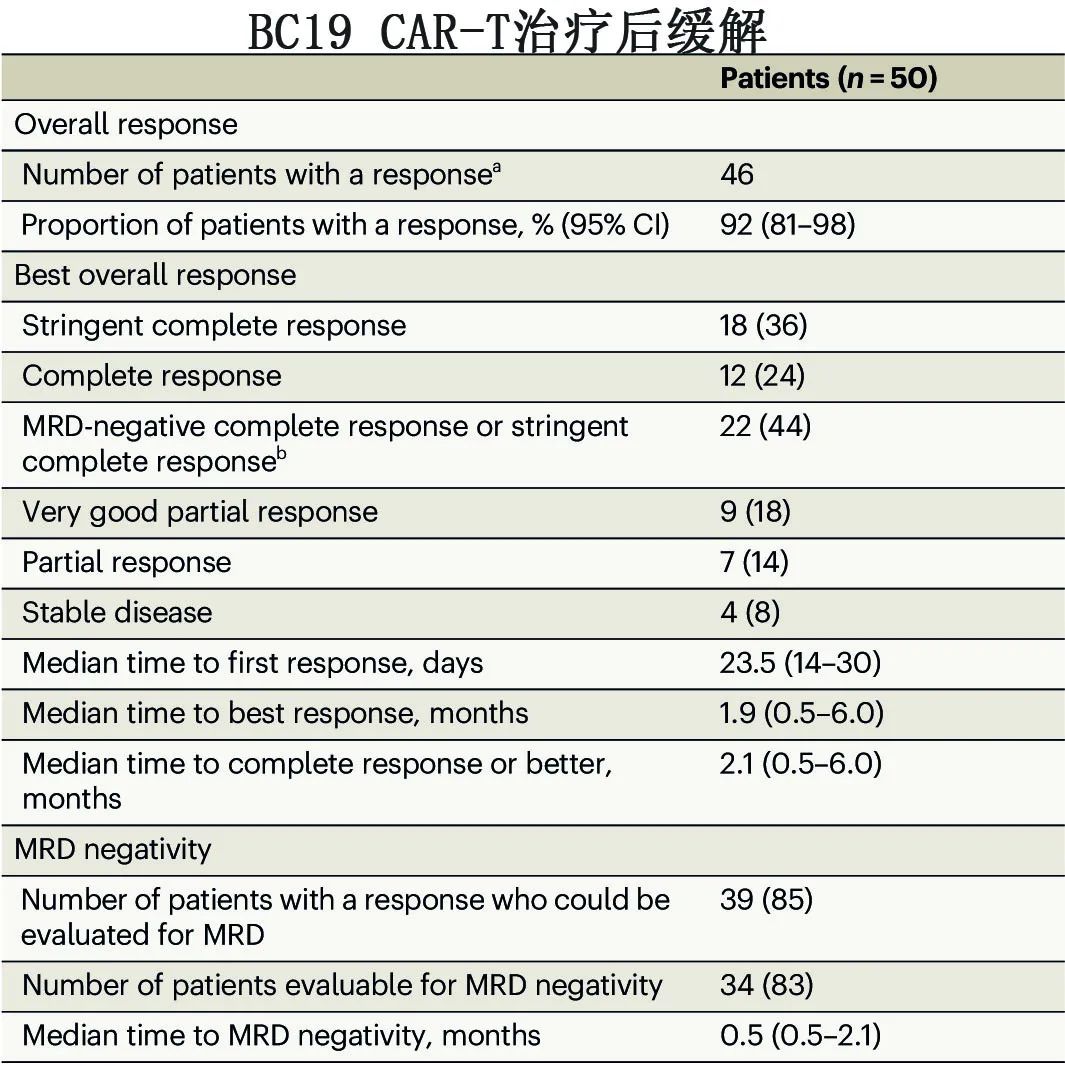
41例进行了MRD检测,其中34例(83%)达到MRD阴性,包括22例CR或sCR(表2)。CAR-T细胞输注后MRD阳性状态变为阴性的患者的中位时间为0.5个月。至MRD阴性时间与缓解深度无关。
单因素分析显示,在关键协变量中ORR一致,包括疾病分期、高危细胞遗传学、髓外病变、基线肿瘤负荷、BCMA表达、CD19检测、既往治疗线数和诊断后时间;但曾接受过CAR-T细胞治疗的患者ORR较低。
中位随访11个月,≥PR的46例患者中有27例(59%) 持续缓解;46例患者中15例(33%)在随访期间出现复发或进展,包括30例≥CR患者中的8例,16例VGPR或PR患者中的7例。
15例复发或进展患者进行了BCMA和CD19检测,其中1例(7%)复发为BCMA阴性骨髓瘤细胞,14例(93%)复发为BCMA阳性骨髓瘤细胞;15例骨髓瘤细胞CD19表达均为阴性。
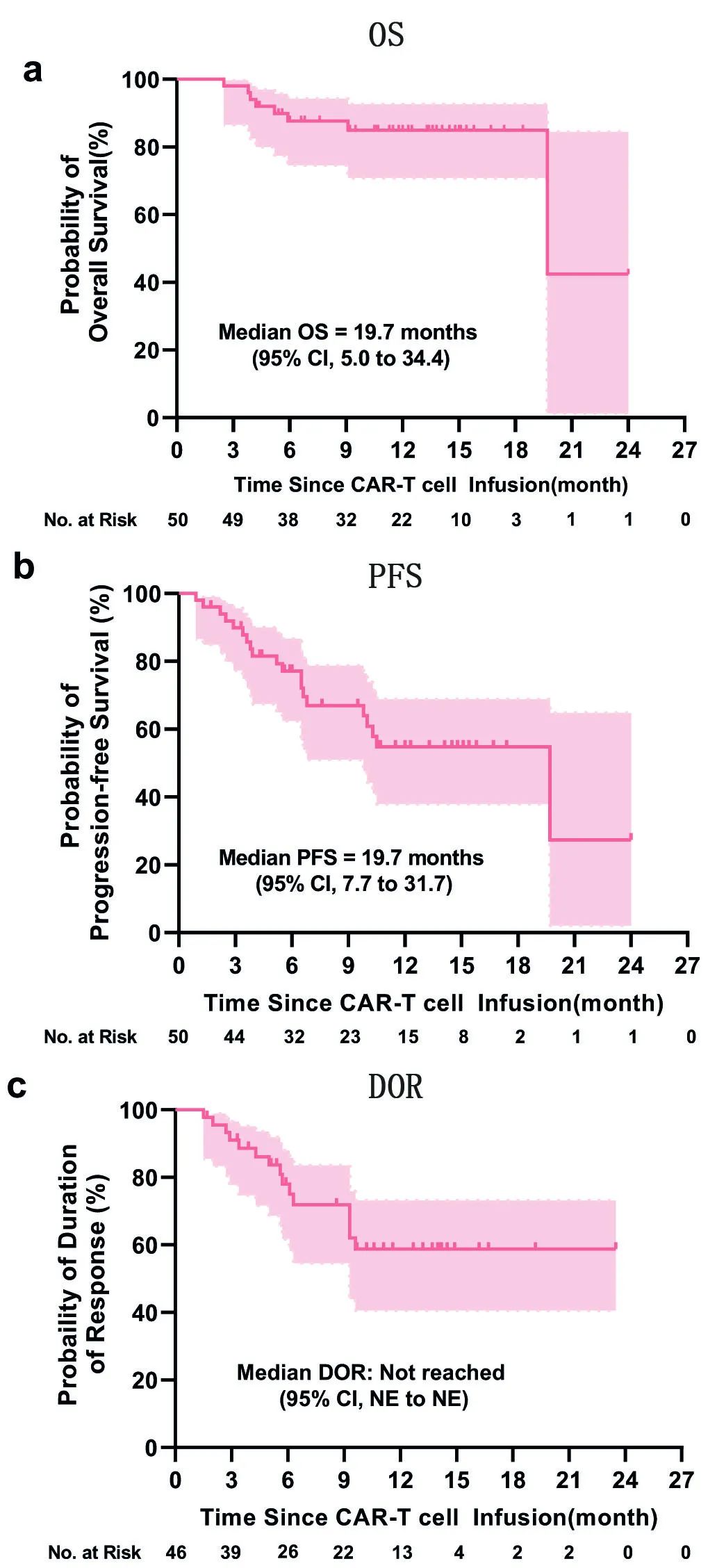
50例患者的中位OS和PFS分别为19.7个月和19.7个月。46例≥PR患者的中位DOR未达到。1年PFS、OS和DOR率分别为55%、85%和59%,而≥CR患者的12个月PFS和OS率分别为66%和90%。
总结
结果耐受性良好,表现出显著的临床疗效。该人群的总缓解率为92%,中位无进展生存期为19.7个月,1年总生存率为85%。8%的患者出现3级或更高级别的细胞因子释放综合征,4%的患者出现1级神经毒性事件,符合预定的主要终点。
总体而言,该研究发现输注 BC19 双特异性 CAR-T 细胞是管理 RRMM 患者的一种可行、安全和有效的策略。还需要更大的样本量和更长的随访时间的前瞻性和多中心研究,以探索BC19 CAR-T细胞治疗对长期结局的影响。
参考文献
Shi, M., Wang, J., Huang, H. et al. Bispecific CAR T cell therapy targeting BCMA and CD19 in relapsed/refractory multiple myeloma: a phase I/II trial. Nat Commun 15, 3371 (2024). https://doi.org/10.1038/s41467-024-47801-8
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#多发性骨髓瘤# #CAR-T# #BCMA# #RRMM#
11