【Blood】如何使用基因组学和BTK抑制剂治疗华氏巨球蛋白血症
2024-01-30 聊聊血液 聊聊血液 发表于陕西省
《Blood》近日发表综述,介绍了基于基因组学、疾病特征和合并症,并通过具体案例描述了初治和经治 WM 患者中BTK 抑制剂的治疗算法。
华氏巨球蛋白血症
华氏巨球蛋白血症 (WM)中常见MYD88和 CXCR4突变,此外部分WM 患者的也携带TP53异常,尤其是既往接受过治疗的 WM 患者。MYD88 突变可上调并激活HCK,驱动 BTK 促生存信号。WM 中CXCR4无义和移码突变均可发生,其中无义突变(如CXCR4S338X)对 BTK 抑制剂表现出更大的耐药性。
共价 BTK 抑制剂 (cBTK-i) 在WM 患者中可产生70-80%的主要缓解(major response)率。MYD88 和 CXCR4 突变状态可影响cBTK-i 治疗的 WM 患者的至主要缓解时间、缓解深度和/或无进展生存期 (PFS)。在MYD88、CXCR4突变或 TP53 异常野生型患者中,cBTK-i泽布替尼显示出更强的缓解活性和/或改善PFS。在 WM 患者中,BTK 抑制剂之间的不良事件存在显著差异,包括房颤、出血倾向和中性粒细胞减少症。c-BTKi 也常见不耐受,可考虑减量或转换为另一种c-BTKi。对于对 c-BTKi 获得性耐药的患者,新的选择包括非共价 BTK-抑制剂pirtobrutinib或 BCL2 拮抗剂维奈克拉。BTK 抑制剂联合化学免疫治疗、CXCR4和 BCL2 拮抗剂的方案也已取得较大进展。
《Blood》近日发表综述,介绍了基于基因组学、疾病特征和合并症,并通过具体案例描述了初治和经治 WM 患者中BTK 抑制剂的治疗算法。

WM的基因组学和BTK抑制剂
MYD88突变
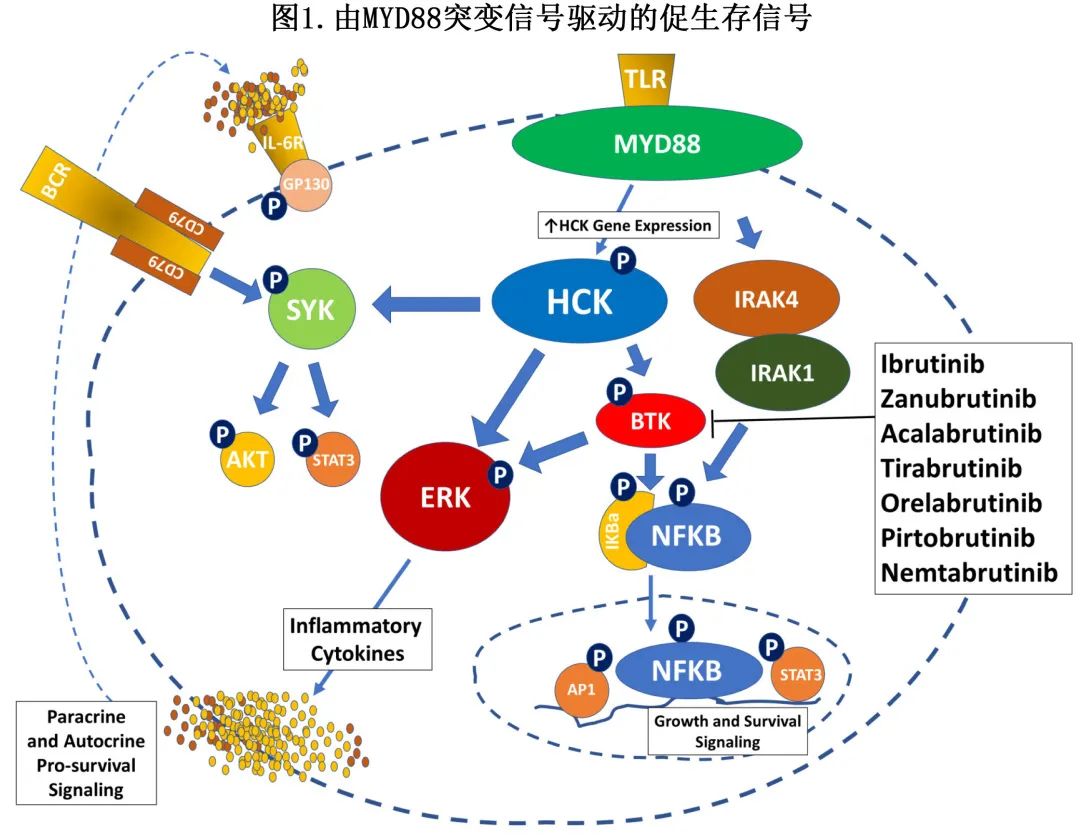
95-97%的 WM 患者存在MYD88突变(MYD88Mut)。几乎所有病例均携带 MYD88L265P变异(variants),但也存在其他 MYD88Mut变异。在35%的 WM 患者中,二代测序 (NGS) 可能遗漏MYD88L265P,特别是在骨髓 (BM) 疾病负荷<10%的患者中,因此推荐 AS-PCR 用于 MYD88L265P检测。MYD88 Mut的信号级联如图1所示。5%的 WM 患者为 MYD88 野生型 (MYD88WT),其中许多患者携带 BTK 信号远端的 NFKB 激活突变。MYD88 WT患者的疾病转化风险较高,和/或总生存期 (OS) 较短。MYD88Mut状态可对 BTK 抑制剂的结局产生不同影响(下文讨论)。因此,建议通过 AS-PCR 确定 MYD88L265P变异的 MYD88Mut状态,作为诊断检查的一部分,如果为阴性,则考虑使用 NGS 识别非 MYD88L265P变异。
CXCR4突变
CXCR4Mut见于30-40%的 WM 患者。已在在 WM 中发现超过40种 C 末端结构域的 CXCR4 无义和移码变异,无义(CXCR4Mut/NS)变异是最常见的CXCR4S338X,可导致 C-末端调节结构域截断。移码 (CXCR4Mut/FS) 变异则由插入或缺失导致。CXCR4Mut 克隆通常为亚克隆。尽管克隆性具有异质性,但CXCR4Mut WM患者的转录谱具有很大的一致性。作为对 CXCL12 的反应,CXCR4Mut可触发BTK、AKT和 ERK 信号,促进 BM 趋化和/或伊布替尼耐药。与表达 CXCR4WT 或 CXCR4Mut/NS 的 WM 细胞相比,表达 CXCR4 Mut/FS 的 WM 细胞表现出更稳健的 AKT 和 ERK 信号转导。CXCR4拮抗剂可使表达 CXCR4Mut 的 WM 细胞对伊布替尼敏感。
与 CXCR4WT 或 CXCR4Mut/FS 突变患者相比,CXCR4Mut/NS WM患者的 BM 疾病负荷更高,血清 IgM (sIgM) 水平和症状性高粘血症的发生率更高,和/或至初始治疗的时间更短。一项研究还表明,CXCR4Mut/NS患者的 OS 短于 CXCR4WT 或CXCR4Mut/FS。CXCR4Mut/NS患者与 CXCR4WT 或 CXCR4Mut/FS 相比,可能对BTK抑制剂的治疗结局产生更多不利影响(见下文)。NGS 可能会遗漏2/3的 CXCR4Mut 患者,特别是 BM 疾病负担和克隆性较低的患者,而较新的 NGS 平台可能会改善检测结果。鉴于 CXCR4Mut/NS 的意义,AS-PCR可用于评价该变异,因此建议将 CXCR4 Mut状态作为 NGS 诊断检查的一部分,如果为阴性,则考虑AS-PCR检测 CXCR4S338X 变异。
TP53异常
5-10%的初治 WM 患者发生 TP53异常(TP53Alt),包括 TP53Mut 和 17p 缺失。TP53 Alt的发生率在经治WM 患者中似乎更高 (25-30%),且其中大多数接受过烷化剂 (85%) 和/或核苷类似物 (22%) 治疗。TP53 Alt WM 患者使用 BTK 抑制剂时 OS 和/或 PFS 更短。建议在诊断时和复发时使用 NGS 评价TP53 Alt,因为其存在可指导治疗考虑(下文讨论)。由于目前的研究均为定性,尚未确定 TP53 Alt的临界值。
BTK突变
BTKCys481是共价 BTK 抑制剂 (cBTK-i,包括伊布替尼、泽布替尼、阿可替尼和 tirabrutinib) 的结合位点,其变异也是获得性伊布替尼耐药 WM 患者中最常见的突变。重要的是,在接受伊布替尼治疗后疾病进展的个体 WM 患者,可能出现多个携带不同 BTK Cys481突变的克隆。与 CLL 一样,在接受 BTK 抑制剂治疗后进展的 WM 患者中,BCyCys481突变通常为亚克隆。表达 BTKCys481Ser突变的 WM 细胞呈伊布替尼耐药性和BTK-PLCγ2-ERK1/2信号转导的再激活。使用 ERK1/2 抑制剂可触发表达 BTKCys481Ser的细胞凋亡,并使伊布替尼重新致敏。此外,ERK1/2再激活伴随 IL6 和 IL-10的释放,可保护共培养的野生型 BTKCys481 WM 细胞免受伊布替尼的影响,证明存在传播 cBTK-i 耐药性的旁分泌方式。在接受伊布替尼治疗后疾病进展的 WM 患者中,也会发生染色体 6q 或8p(包括BTK、MYD88/NFκB调节因子)和凋亡信号传导的缺失。由于挽救性治疗(下文讨论)未根据 BTKCys481 突变状态评价结局,因此建议对接受 cBTK 抑制剂治疗后进展的 WM 患者进行常规 BTKCys481变异检测。
WM中BTK抑制剂的临床经验
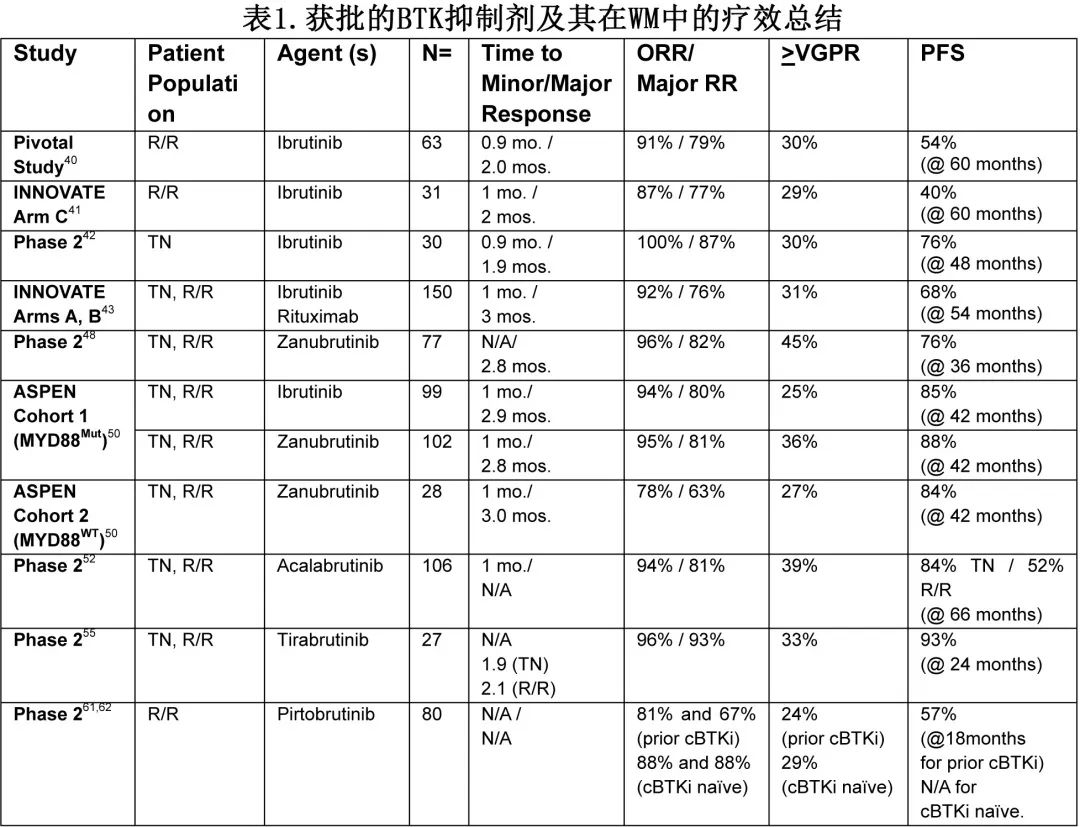
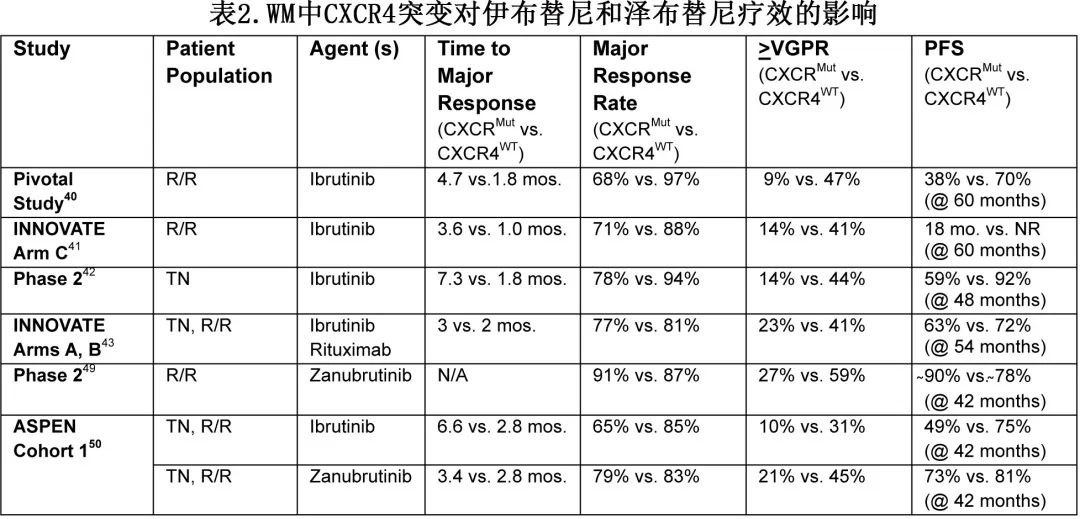
表1总结了WM 中使用 BTK 抑制剂的研究。表2总结了CXCR4Mut 状态对伊布替尼和泽布替尼结局的影响。原文对于研究的详细解读不做赘述,下文直接翻译作者通过具体案例阐述的治疗算法。
WM中BTK抑制剂的定位
案例1:新诊断WM伴症状性高粘血症
患者为42岁男性,因视物模糊、流鼻血就诊。体格检查示视网膜出血,明显的腋窝和腹股沟腺病,脾大。全血细胞减少。血清蛋白电泳(SPEP)示IgMλ单克隆蛋白,sIgM为12400 mg/dL。CT表现为弥漫性大肿块腺病。骨髓活检示80%淋巴浆细胞(LPL)受累,分子诊断示MYD88L265P和CXCR4S338X突变。
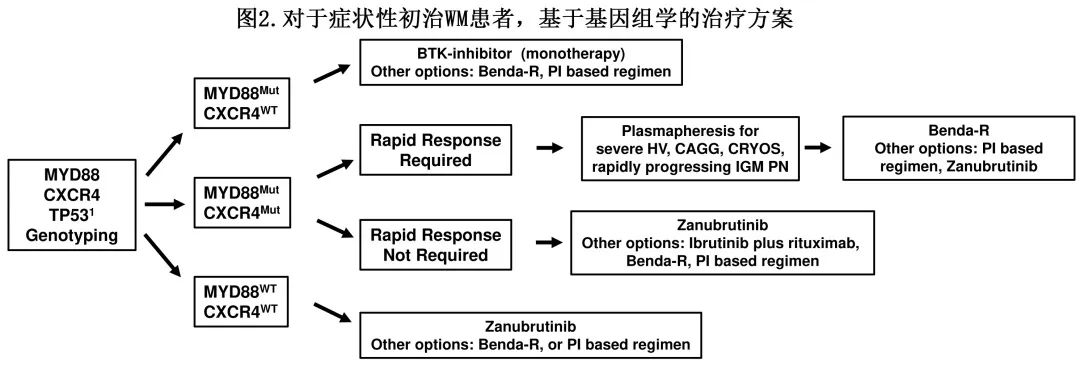
图2为症状性初治 WM 患者的治疗算法,下文提出的建议则考虑了最近的共识小组指南。对于症状性初治患者,可考虑使用Benda-R、地塞米松、利妥昔单抗和环磷酰胺 (DRC) 以及 BTK 抑制剂进行免疫化疗。对于免疫化疗,作者倾向于 Benda-R 而非DRC,因为前者可能提供更深的缓解和更长的PFS。考虑到两项回顾性研究的结果(包括在症状性初治 WM 患者中进行的一项专门研究,结果显示与4个号额6个周期相比结局没有差异),作者倾向于在可能的情况下使用4个周期来最小化短期和长期不良事件。治疗大体积疾病或症状性淀粉样变性时,则支持使用长达6个周期的Benda-R。作为这些建议的一部分,作者考虑了一项多中心、回顾性研究,其中开始给药取决于当地实践,并显示接受苯达莫司汀>1000 mg/m2的一线患者在达到主要缓解和 PFS 方面具有获益。但在复发/难治性患者中未观察到此类获益。
对于>70岁或 EGFR 低表达患者,应考虑减少苯达莫司汀的剂量。关于 BTK 抑制剂与免疫化疗相对疗效的数据很少。一项纳入246例初治 MYD88Mut WM 患者的多中心、回顾性研究比较了 Benda-R 与伊布替尼的结局,7%的患者接受>4个周期的Benda-R,中位随访时间为4.2年。Benda-R 组的主要缓解(92% vs. 83%)、VGPR(50% vs. 33%) 和CR(20% vs. 2%) 率均高于伊布替尼组,但PFS 和 OS 相似,支持 BTK 抑制剂与 Benda-R 具有相当的长期疾病控制。
对于仅 MYD88Mut患者,作者倾向于cBTK-i,以尽量减少获得性 TP53Alt 的风险,因为所有 cBTK-i 在仅 MYD88Mut 患者疗效相似(表1),因此选择应考虑表3中提供的可及性和指导。对于需要快速缓解的 CXCR4Mut 患者(例如病例1),Benda-R或泽布替尼可能较合理。有症状的高粘血症者应考虑血浆置换。如果选择Benda-R,应暂停利妥昔单抗治疗直至 sIgM <4000 mg/dL,以避免触发高粘血症危象。需要快速缓解的 CXCR4Mut 患者中也可考虑泽布替尼。在 ASPEN 研究中接受泽布替尼治疗的 CXCR4 Mut WM 患者的中位至主要缓解时间为2.8个月,与 Benda-R 相当。对于病例1来说,Benda-R更适合,因为缺乏 BTK 抑制剂治疗大体积疾病的数据。
对于不需要快速控制疾病的 CXCR4Mut 患者,可以考虑使用泽布替尼,因为与伊布替尼相比具有更短的至主要缓解时间、更深的缓解和更长的PFS。对于 MYD88WT 患者,由于可实现高水平缓解和长期疾病控制,因此支持泽布替尼用于症状性初治患者。Benda-R 和蛋白酶体抑制剂 (PI) 为基础的治疗是 CXCR4Mut 或 MYD88WT 患者的替代方案。在确定 BTK 抑制剂时可考虑 TP53Alt 状态;鉴于 ASPEN 研究结果显示,泽布替尼较伊布替尼具有更高疗效和长期疾病控制,作者更偏向于 TP53Alt WM 患者使用泽布替尼。
案例2:需要治疗的经治高危WM患者
患者为42岁女性,因头痛、视物模糊就诊。检查示 sIgM 单克隆蛋白;sIgM水平>10000 mg/dL;BM LPL受累85-90%。分子学检查示MYD88L265P、CXCR4V340FS和 TP53Y163C 突变。血红蛋白为9.9 g/dL,血小板计数为72000 K/uL。患者接受硼替佐米、地塞米松和利妥昔单抗 (BDR) 治疗后部分缓解,但1.5年后进展。然后在临床试验中接受维奈克拉,但治疗3个月后无反应。
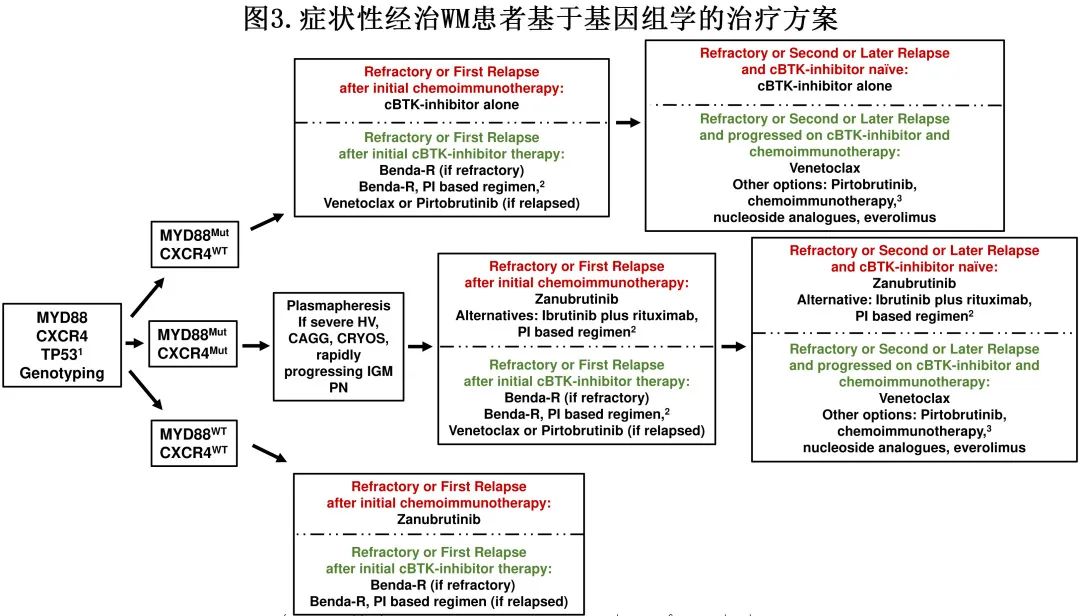
图3为症状性经治 WM 患者的治疗算法,相关建议也审议了最近的共识小组指导。专家组指出,在治疗选择中应考虑生物学年龄、合并症和健康状况、复发性质、患者偏好、造血功能储备和突变状态 (MYD88、CXCR4、TP53)。对于仅 MYD88Mut的难治性或初始免疫化疗后首次复发的患者,应考虑cBTK-i。由于所有 cBTK-i 在仅 MYD88Mut 患者中表现出相似的疗效(表1),药物选择应考虑表3中提供的可及性和指导。对于初始免疫化疗后难治或首次复发的 MYD88Mut CXCR4Mut 患者,作者首选泽布替尼。对于MYD88WT WM患者,泽布替尼也是初始免疫化疗后的推荐治疗。TP53Alt WM患者也首选泽布替尼,正如案例2为MYD88Mut CXCR4Mut TP53Alt。
对于停用伊布替尼的患者,免疫化疗的ORR为73%,且伊布替尼停药2周内开始免疫化疗的患者缓解率更高。由于停用 BTK 抑制剂后 sIgM 反弹很常见,因此对于 sIgM 水平较高的患者,可以考虑采用桥接策略,即继续使用 BTK 抑制剂,直至通过免疫化疗实现疾病控制。
对于初始cBTK-i治疗难治的患者,无论基因组亚型如何,均推荐使用Benda-R。如果选择Benda-R,应暂停利妥昔单抗治疗直至sIgM<4000 mg/dL,以避免触发高粘血症危象。对于初始 cBTK-I 缓解后进展的患者,可选治疗包括Benda-R、PI为基础的治疗、维奈克拉或pirtobrutinib。作者倾向于尽可能降低烷化剂暴露,尤其是<70岁或携带TP53Alt的患者中。对于这些患者,首选维奈克拉,因为其在既往暴露于 cBTK-i 或 CXCR4Mut的WM患者中具有高度活性。但维奈克拉在MYD88WT或TP53Alt WM患者中的活性仍有待明确。Pirtobrutinib是 cBTK-i 治疗后的另一种选择,但其在MYD88WT或MYD88Mut CXCR4Mut患者中的疗效尚不清楚。在接受cBTK-i治疗后进展的患者中也可考虑基于Benda-R或PI的治疗方案,因其对所有基因组亚型均有疗效。第二次或后续复发的其他选择包括:如果缓解持续>3年则再次使用化疗、其他免疫化疗、核苷类似物或依维莫司。复发患者应优先考虑临床试验。
对于患有大包块髓外病变的患者,例如病例1,Benda-R更适合,因为缺乏 BTK 抑制剂在大包块疾病患者中的数据。对于伴症状性淀粉样变性的 WM 患者,建议在合适的患者选择用基于 Benda-R 或 PI 的治疗序贯大剂量化疗和自体干细胞移植巩固治疗。接受伊布替尼或阿可替尼治疗的少数病例的结果显示 PFS 较短及出血和房颤更明显。鉴于广泛报道显示 BTK 抑制剂的疗效和持久性,Bing Neel 综合征(BNS)患者可优先使用 BTK 抑制剂。
BTK抑制剂不耐受或耐药WM的治疗
案例3:伊布替尼治疗的患者VGPR但发生房颤
73岁男性出现疲乏,血红蛋白为9.1 g/dL。检查示 sIgM 单克隆蛋白;sIgM水平为2301 mg/dL。BM 活检示 LPL 受累50%,仅检测到 MYD88L265 突变。CT 扫描示弥漫性腺病(最大淋巴结2.3 cm)和轻度脾肿大。开始使用伊布替尼并达到VGPR。在开始伊布替尼治疗后1年,患者发生症状性房颤伴快速心室反应。淀粉样蛋白沉积的心脏检查无明显异常。开始接受美托洛尔治疗,并接受阿哌沙班抗凝治疗。心脏复律但仍有多次房颤发作。还出现血尿和瘀斑,接受抗凝治疗。
伊布替尼不耐受的停药率约为30%。在中位随访64个月的353例 WM 患者中评价了伊布替尼的剂量降低,96例 (27%) 因不良事件需要降低剂量,且剂量降低在65岁以上和女性中更常见。减量后大多数患者 (65%) 的不良反应改善或消退,大多数 (79%) 患者的血液学缓解持续或加深,10例房颤患者中仅1例在减量后心律失常未复发。对于发生伊布替尼相关房颤的 WM 患者,例如病例3,换用另一种BTK抑制剂更为合适。在一项纳入 WM 患者的研究中,研究了使用泽布替尼治疗伊布替尼或阿可替尼不耐受的患者,结果伊布替尼 (70%) 和阿可替尼(83%) 的大多数不耐受事件在泽布替尼转换后未复发。在10例因房颤转换治疗的患者(均来自伊布替尼)中,9例未复发。转换为泽布替尼治疗后,长期疾病控制率为94%。应尽快启动转换治疗,以防止 sIgM 反弹。从伊布替尼转换为阿可替尼的数据有限,2例 CLL 患者中有1例发生房颤复发。
案例4:既往多线治疗且在伊布替尼治疗期间进展的WM患者
患者男,55岁,13年前因贫血、乏力就诊后诊断为WM。诊断时血红蛋白为9.6 g/dL,sIgM为2800 mg/dL,BM活检示90%受累,CT 扫描无异常。患者对环磷酰胺、泼尼松和利妥昔单抗、Benda-R、硼替佐米/地塞米松和依维莫司的反应极小或无反应。随后患者开始接受伊布替尼 420 mg/dL 治疗并达到VGPR。11年后患者出现疲乏,血红蛋白为7.1g/dL。BM 活检示95%的 LPL 受累,和两种不同的BTKCys481 (c.1442G>c;c1441 T>A) 突变。
对于BTKCys481 突变相关获得性 c-BTK-I 耐药的患者,如病例4,不建议转换为另一种c-BTK-I。对于既往暴露于 cBTK-i 的患者可考虑使用Pirtobrutinib,MRR 为66%,PFS为19.4个月,但携带 BTK Cys481突变患者的具体数据还未出结果。维奈克拉也是一种选择,在既往暴露于 BTK 抑制剂或 CXCR4Mut 疾病的 WM 患者中具有疗效,在既往暴露于 cBTK-i 的患者中观察到的ORR(76% vs. 93%) 和MRR(76% vs. 87%) 低于无 c-BTK-i 暴露的患者,但未观察到 PFS 的显著差异。此外如上所述,对 c-BTK-i 不耐受或进展的患者也可考虑免疫化疗。其他挽救治疗选择见图3。作者治疗c-BTK-i 获得性耐药的 WM 患者的偏好是使用非共价 BTK 抑制剂,如pirtobrutinib(如可用),然后类别转换为 BCL2 抑制剂,如维奈克拉。对于接受 BTK 和 BCL2 抑制剂治疗后疾病进展的患者,可考虑选择化疗或临床试验。
WM中选择BTK抑制剂的考虑因素
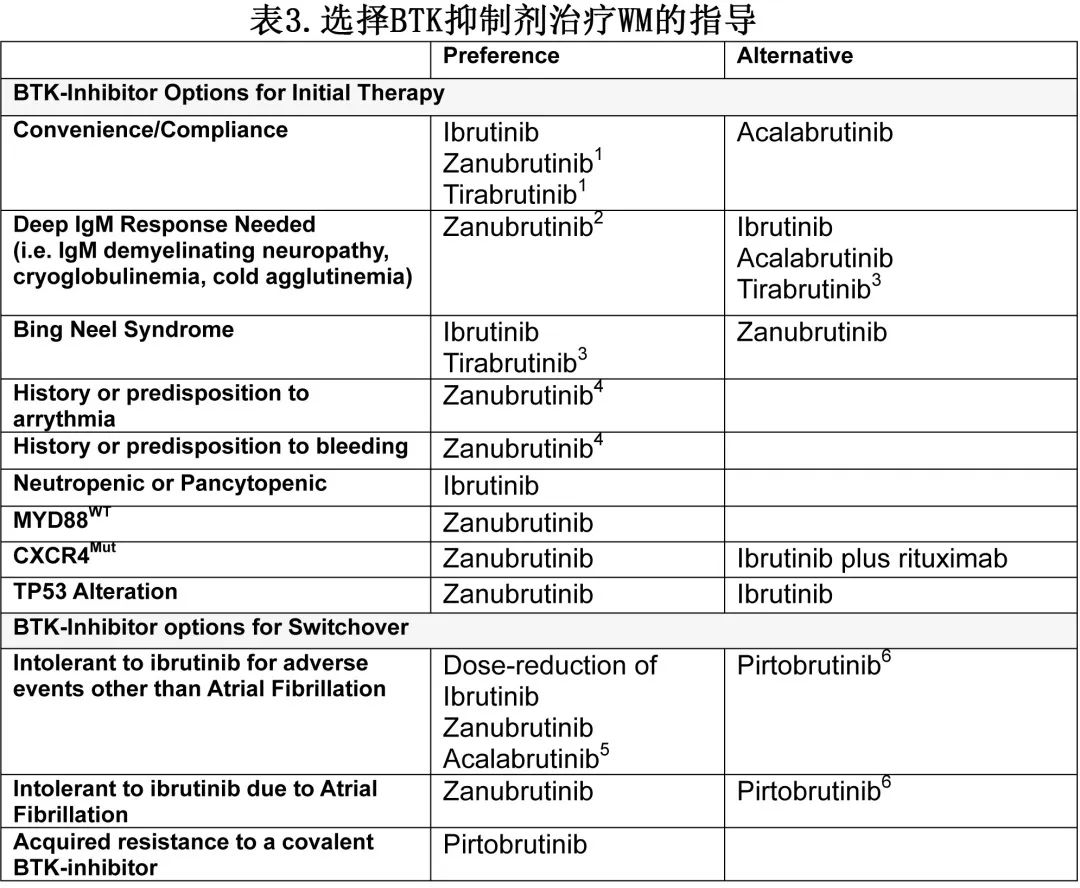
在选择 BTK 抑制剂时,应考虑依从性、疾病表现的性质、合并症、突变状态 (MYD88、CXCR4、TP53、BCysTK481) 以及对 cBTK-i 的耐受性和获得性耐药。表3总结了患者和疾病特征,包括为 WM 选择 BTK 抑制剂时的基因组学。
与BTK抑制剂相关的戒断症状
接受伊布替尼治疗的 WM 患者中20%可出现戒断症状,症状通常在伊布替尼暂停后2天内发生,并在重新开始治疗后迅速消退。在伊布替尼后出现戒断症状的患者中,2/3在停药期间没有疾病进展的证据。戒断症状包括发热、身体疼痛、盗汗、关节痛、寒战、头痛和疲劳。当伊布替尼停药时,也可能发生 sIgM 反弹。关于其他 BTK 抑制剂戒断症状或 sIgM 反弹的报告有限。
参考文献
Treon SP, et al.How we use Genomics and BTK-Inhibitors in the Treatment of Waldenstrom Macroglobulinemia.Blood . 2024 Jan 11:blood.2022017235. doi: 10.1182/blood.2022017235.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#BTK抑制剂# #华氏巨球蛋白血症#
33