药物引起的 QT 间期延长及其急性过量并发症的案例研究和报告的系列指南
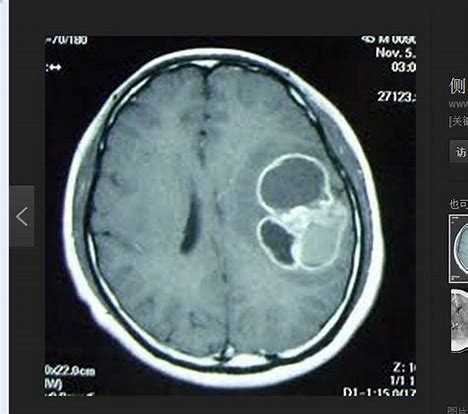
背景:对于中毒引起 QT 间期延长的患者,评估和管理需要采用适当的方法来测量和调整心率(HR),以判断患者是否面临危及生命的心律失常风险,特别是扭转型室性心动过速。在临床毒理学协作(CTC)工作组审查
BIAS:生物医学图像分析挑战的透明报告
每年组织的生物医学图像分析挑战赛的数量正在稳步增加。 这些国际竞赛的目的是在通用数据集上对算法进行基准测试,通常是为了确定针对给定问题的最佳方法。 然而,最近的研究表明,与挑战报告相关的常见做法不允许
加强药物遗传学研究的报告:STROPS 指南的制定
背景:通常需要大样本量来检测药物遗传学标记物与治疗反应之间具有统计学意义的关联。 可以进行荟萃分析来综合多项研究的数据,增加样本量,从而提高检测显着遗传效应的能力。 然而,由于研究报告中关键数据的报告
临床人工智能建模的最少信息要求:MI-CLAIM 检查表
由于机构的患者隐私政策,原始临床数据的共享通常是不可能的,如果没有此类保障措施,也不建议共享原始临床数据。 此外,能够对临床数据进行新分析的相同方法也可能以有时不可预测的方式重新识别患者17。 无论如
TIDieR-Placebo:报告安慰剂和假对照的指南和清单
背景:安慰剂或假对照是衡量许多主动干预措施的益处和危害的标准。 虽然成分及其递送方法已被证明会影响研究结果,但安慰剂和假对照很少有报道,并且通常与活性比较剂不匹配。 这可能会影响主动干预的有益或有害程
麻醉病例报告 (ACRE) 检查表:促进围手术期实践高质量病例报告的工具
病例报告在麻醉的发展中发挥了重要作用,并继续与现代实践高度相关。 尽管如此,它们有时仍因不够严格而受到批评,无法为临床实践或研究设计提供有意义的信息。 报告清单是提高研究严谨性的有用工具,尽管之前已经
儿科牙科研究报告标准 (RAPID):专家共识
目前可提供针对不同研究设计的报告指南,以准确、透明地报告研究。 有必要制定针对儿童牙科领域的补充指南。 本研究旨在使用预先定义的基于专家共识的 Delphi 流程,制定儿科牙科 (RAPID) 指南研
中医药病案报告发表规范专家共识(CARC)
病例报告是中医宝贵的临床证据。 然而,总体报告质量并不理想。 成立了一个由20名成员组成的工作组,负责制定中医病例报告(CARC)的系统建议。 工作组(CARC小组)在审查中医病例报告的总体报告质量和
流行病预测和预测研究推荐报告项目:EPIFORGE 2020指南
几十年来包括 COVID-19 在内的传染病暴发凸显了传染病流行预测和预测研究的重要性。 与临床试验和系统评价等其他医学研究领域不同,尽管流行病预测和预测研究很实用,但并不存在报告指南。 因此,我们制
实施 27 项 PRISMA 2020 声明项目,用于运动和运动医学、肌肉骨骼康复和运动科学领域的系统评价:PERSiST(在运动、康复、运动医学和运动科学中实施 Prisma)指南
医疗保健系统评价报告不力是运动和运动医学、肌肉骨骼康复和运动科学领域也无法幸免的一个问题。 透明、准确和全面的系统评价报告有助于研究人员复制方法,读者了解所做的事情和原因,以及临床医生和政策制定者在实
龋齿检测和诊断性研究的标准报告 (STARCARDDS)
目的:本文的目的是提出国际研讨会的建议,该研讨会评估了龋齿诊断研究的方法和报告。 作为一个独特的特征,此类研究的重点是龋齿病变的检测和评估,并且其中许多研究是在体外进行的,因为可以对整个龋齿谱进行组织
【中文】ICH指导原则:质量风险管理Q9(R1)
本文件为企业和监管部门提供质量风险管理的原则以及一些质量风险管理工具,这些原则和工具促进企业和监管机构对原料药及制剂(药品)在其生命周期中的质量做出更有效和一致的基于风险的决策。
重症监护病房中潜在药物相互作用识别的异质性:系统回顾、严格评估和报告建议
入住重症监护病房 (ICU) 的患者经常暴露于潜在的药物相互作用 (pDDI)。 然而,不同研究报告的 ICU 中 pDDI 发生率差异很大。 这可以部分地通过他们的方法论的显着差异来解释。 深入了解